Ma, a parte un thread nella sezione dei congressi, in cui raccontavo per esteso una sua lezione al CROI 2013 sulle ultime scoperte nel campo della patogenesi dell'HIV e dell'SIV - [CROI 2013]G.Silvestri: Nuova comprensione della patogenesi - non avevo ancora avuto l'occasione di dedicare a Silvestri un thread tutto suo, proprio perché i suoi studi scorrono in genere su un piano sottostante agli studi sui farmaci e le strategie di cura, che sono gli argomenti che trattiamo di preferenza in questo forum, ma che senza la ricerca di base neppure esisterebbero.
Ieri, però, è uscito su PLOS PATHOGENS un articolo relativo a una ricerca di Silvestri, che serve a portare luce sulle ragioni che hanno permesso la cura dell'infezione in Timothy Brown e di cui ho già parlato di sfuggita la primavera scorsa, quando Maud Mavigner, una collaboratrice di Silvestri, ha partecipato a una "discussione a tema" al CROI sui trapianti di midollo.
Posso quindi finalmente dare inizio a un thread riservato alle ricerche di Guido Silvestri, e appena possibile parlerò qui anche di un altro filone di ricerca da lui seguito, quello dei CD4 memoria con caratteristiche di staminali, che si stanno rivelando come un importante reservoir di HIV latente.
Il lavoro su PLOS PATHOGENS s'intitola Persistence of Virus Reservoirs in ART-Treated SHIV-Infected Rhesus Macaques after Autologous Hematopoietic Stem Cell Transplant e per la sua importanza si è meritato un articolo di Jon Cohen nella sezione News di Science (How did the 'Berlin patient' rid himself of HIV?).
Che cosa, fra i diversi trattamenti ricevuti dal Berlin Patient, abbia contribuito maggiormente nel condurre a una cura è questione tutt’ora oggetto di dibattito fra gli scienziati. Tre sono le componenti considerate cruciali e non si può escludere che una combinazione di due o tutte e tre queste componenti sia alla base del successo nella cura:
- [divbox]1. IL COMPLESSO REGIME DI CONDIZIONAMENTO MIELOABLATIVO CUI TIMOTHY È STATO SOTTOPOSTO PRIMA DEL TRAPIANTO (CHEMIOTERAPIA, RADIOTERAPIA E SIERO ANTILINFOCITARIO), CHE HA DISTRUTTO QUASI TUTTO IL SISTEMA IMMUNITARIO;
2. LE STAMINALI RICEVUTE DA UN DONATORE OMOZIGOTE PER LA DELEZIONE Δ32 DEL GENE CHE CODIFICA PER IL RECETTORE CCR5, CHE HANNO GENERATO UN SISTEMA IMMUNITARIO REFRATTARIO ALL’HIV;
3. LA GRAFT VERSUS HOST, CHE PUÒ AVERE DISTRUTTO EVENTUALI CELLULE RESIDUE CONTENENTI VIRUS LATENTE E AVERE QUINDI AVUTO UN EFFETTO NON SOLO CONTRO LA LEUCEMIA, MA ANCHE CONTRO IL RESERVOIR DI HIV.[/divbox]
Lo studio sui Boston Patients, che hanno ricevuto staminali CCR5 wild type dopo un condizionamento più leggero di quello di Timothy e, quando hanno sospeso la ART, hanno sì avuto un rebound delle viremie, ma differito rispetto alle attese, ha contribuito a rafforzare l’importanza delle staminali CCR5 negative.
D’altra parte, lo studio di Mellors degli effetti del trapianto autologo di staminali sull’RNA e il DNA virali ci ha detto che la Graft - che ovviamente negli autotrapianti non si verifica – potrebbe avere contribuito in misura determinante al successo del Berlin Patient (benché nei Boston Patients ci sia stata, senza però essere risolutiva).
L’interesse di quest’ultimo lavoro di Guido Silvestri consiste nell’aver cercato di stabilire il contributo del terzo fattore in gioco nella distruzione del reservoir virale, quello del condizionamento mieloablativo mediante irradiazione, e nell’averlo fatto costruendo un modello di trapianto autologo in macachi affetti da SHIV (un virus chimera, in parte SIV, in parte HIV), con viremia soppressa da un potente regime di ART (2 NRTI, tenofovir e emtricitabina + 1 NNRTI, efavirenz + 1 INSTI, raltegravir).
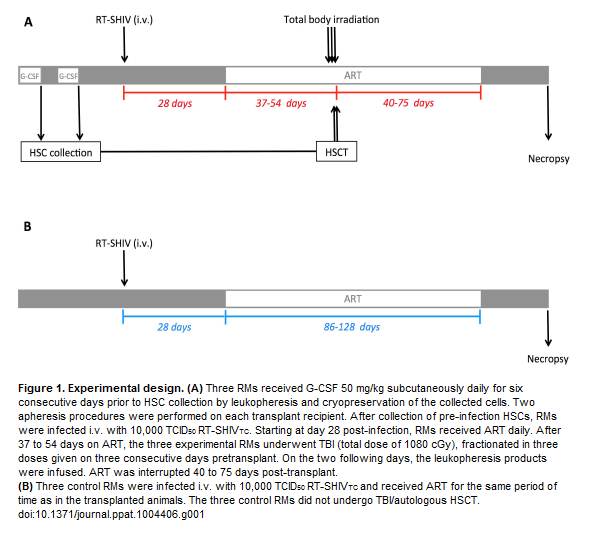
I macachi rhesus erano 6: a 3 scimmie sono state prelevate le staminali, poi tutti e 6 gli animali sono stati infettati e, una settimana dopo, hanno cominciato la ART.
Dopo essere state infettate, tutte e 6 le scimmie hanno avuto un aumento rapido ed esponenziale della replicazione virale, che ha raggiunto il picco a 2 settimane dall’infezione. La ART iniziata a 4 settimane ha rapidamente ridotto la viremia sotto le 100 copie di SHIV RNA/mL di plasma. Come si è già visto in altri modelli di infezione dei macachi con SHIV, il numero dei CD4 è diminuito e poi è stato parzialmente recuperato con la ART.
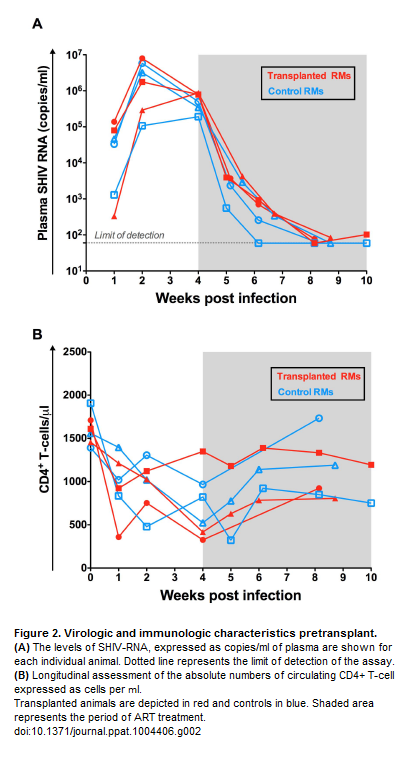
Fra 5 e 8 settimane dopo, 3 macachi hanno ricevuto una total body irradiation (TBI) che ha distrutto il loro midollo (drastica riduzione di tutte le cellule del sangue, dalle piastrine, per le quali poi sono state fatte trasfusioni, a neutrofili, monociti, e linfociti – distruzione del 94-99% dei CD4 circolanti). Poi sono state loro infuse le staminali precedentemente prelevate. Quando, fra 5 e 11 settimane dopo il trapianto, si è visto che le cellule avevano attecchito, i 3 macachi trapiantati e i 3 controlli hanno tutti sospeso la ART.
Veniamo così agli effetti dell’irradiazione pre-trapianto sulla replicazione di SHIV e sul reservoir virale.
Prima ancora di sospendere la ART, subito dopo la TBI e l’infusione delle staminali i 3 macachi trapiantati hanno avuto qualche transitorio blip viremico, verosimilmente proveniente da qualche reservoir sopravvissuto al condizionamento o dovuto al troppo breve periodo di ART, insufficiente a ottenere una soppressione completa della replicazione virale.
Blip a parte, la ART da sola è riuscita a ridurre il livello di SHIV DNA nelle PBMC (cioè nel reservoir periferico): di 1-1,5 log negli animali di controllo, in modo più consistente negli animali trapiantati (2 su 3 sotto il livello di rilevabilità dei test, uno appena al di sopra).
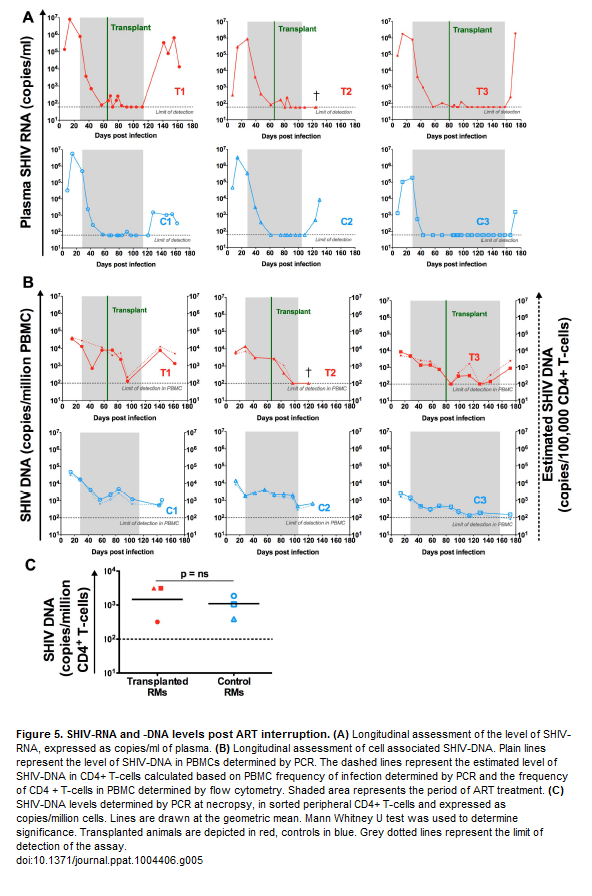
Quando poi , fra 78 e 128 giorni dopo l’infezione, la ART è stata sospesa, come era previsto, le scimmie di controllo hanno avuto un rebound virale nel giro di una settimana.
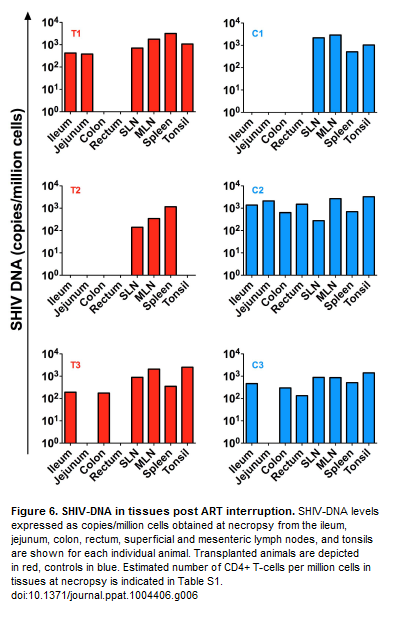
Mentre le scimmie trapiantate, finché sono rimaste sotto antiretrovirali, avevano la viremia non rilevabile nel plasma e il DNA virale o assente o bassissimo nelle PBMC, è bastato sospendere la ART perché 2 scimmie su 3 avessero un rebound della viremia nel giro di pochi giorni, esattamente come i controlli. Il terzo macaco (quello chiamato T2), dopo la sospensione della ART, non ha avuto un rebound di SHIV RNA e aveva dei livelli rilevabili, ma molto bassi, di SHIV DNA nei CD4 del sangue, nella milza e nei linfonodi, mentre non ne aveva nel tratto gastrointestinale e nelle tonsille. Ma sfortuna ha voluto che intervenissero dei problemi renali e dovesse essere soppresso come gli altri.
In sintesi, quello che Silvestri ha scoperto con questo studio è che
- [divbox]1. È POSSIBILE FARE TRAPIANTI AUTOLOGHI DI STAMINALI RACCOLTE PRIMA DELL’INFEZIONE IN MACACHI RHESUS INFETTI DA SHIV (e quello costruito da Silvestri è un modello estremamente complesso - il primo che sia stato fatto - che ha dimostrato di funzionare e potrà essere usato per sperimentare in vivo sia trapianti autologhi dopo periodi di ART molto più lunghi, sia altri tipi di interventi di cura);
2. IL CONDIZIONAMENTO CON IRRADIAZIONE HA COMPORTATO UNA DISTRUZIONE MASSICCIA DEI CD4 CIRCOLANTI;
3. LE SCIMMIE CHE HANNO RICEVUTO IL TRAPIANTO AUTOLOGO SOTTO ART HANNO AVUTO UN RAPIDO E CONSISTENTE DECLINO DEL RESERVOIR NEL SANGUE PERIFERICO E HANNO MANTENUTO VIREMIA IRRILEVABILE, CON LA SOLA ECCEZIONE DI SPORADICI BLIP;
4. 2 DELLE 3 SCIMMIE TRAPIANTATE HANNO AVUTO UN REBOUND QUASI IMMEDIATO DELLA VIREMIA DOPO L’INTERRUZIONE DELLA ART;
5. LA TERZA SCIMMIA, A DUE SETTIMANE DALLA SOSPENSIONE DELLA ART, NON AVEVA VIRUS RILEVABILE NEL PLASMA, NELLE PBMC, NELLE TONSILLE E NELL’INTESTINO, AVEVA BASSI LIVELLI DI DNA VIRALE NEI CD4 E NEI LINFONODI E LIVELLI UN POCO PIÙ ALTI NELLA MILZA.[/divbox]
Il limite maggiore di questa ricerca, insieme al piccolo numero di animali studiati, è che tutto è stato fatto in tempi ridotti e quel che si è potuto valutare è stato solo l’impatto del condizionamento sul reservoir. Se il periodo in cui le scimmie hanno preso la ART fosse stato più lungo, sarebbe stato possibile raccogliere dati anche sull’effetto congiunto di un condizionamento mieloablativo e di una soppressione virale prolungata. E forse, in quel caso, il reservoir latente sarebbe stato molto più ridotto, quindi il rebound virale di molto differito (come accadde nei Boston Patients).
In conclusione, nel caso del Berlin Patient, alla total body irradiation sono state aggiunte la chemioterapia e la globulina antitimocitaria. Quindi il regime di condizionamento è stato più complesso e, probabilmente, più efficace. Ma la TBI ha comunque avuto un effetto importante sulla distruzione del reservoir dei CD4 circolanti nel sangue, anche se non è stata sufficiente ad eliminare tutti i reservoir.
Questo ci dice che, nel contesto di un breve periodo di ART, la distruzione massiccia del comparto ematopoietico che si può ottenere con un condizionamento mieloablativo non è sufficiente a distruggere tutti i reservoir latenti.