Inizio con il nuovo farmaco di Bristol-Myers Squib, perché è il primo di una nuova classe di farmaci, gli inibitori dell’aggancio, mentre in un altro post parlerò del 744 di GlaxoSmithKline, che è un nuovo inibitore dell’integrasi (analogo del dolutegravir) ed è stato studiato insieme alla rilpivirina come terapia di mantenimento, oppure in una formulazione iniettabile pensata per la PrEP.
Jay Lalezari, Quest Clinical Research, San Francisco, ha presentato lo studio di fase IIb sul BMS-663068.

Attachment Inhibitor Prodrug BMS-663068 in ARV-Experienced Subjects: Week 24 Analysis
Inibire l’aggancio dell’HIV alla cellula significa intervenire in una fase ancora più iniziale rispetto all’inibizione dell’ingresso: il maraviroc (Celsentri), che è un inibitore del CCR5, e l’enfuvirtide (Fuzeon), che è un inibitore della fusione, agiscono in un momento leggermente successivo.
BMS-663068 è un pro-farmaco che, quando viene metabolizzato dall’organismo, si trasforma nell’agente attivo BMS-626529, che si lega alla proteina gp120 sulla envelope dell’HIV, bloccando l’interazione fra il virus e la cellula. In breve, BMS-663068 modifica la forma di questa glicoproteina virale, rendendola incapace di collegare l’HIV ai recettori sulla superficie dei CD4. Un aspetto interessante è che, a differenza del maraviroc, BMS-663068 funziona indipendentemente dal tropismo del virus, cioè sia con virus che usano come co-recettore il CCR5, sia con virus che usano il CXCR4.
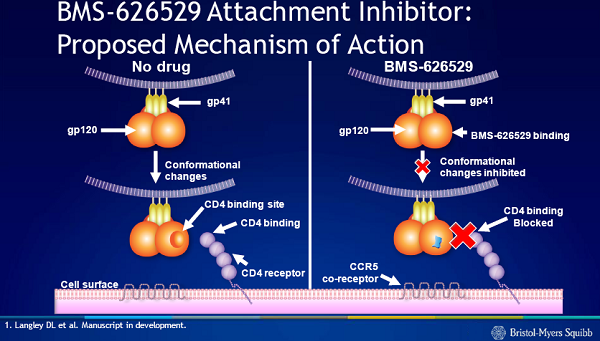
Grazie al fatto che usa un meccanismo di azione nuovo, questo farmaco ha un profilo di resistenza unico, non ha resistenze crociate ed è attivo contro ceppi di HIV che sono resistenti ad altri antiretrovirali.

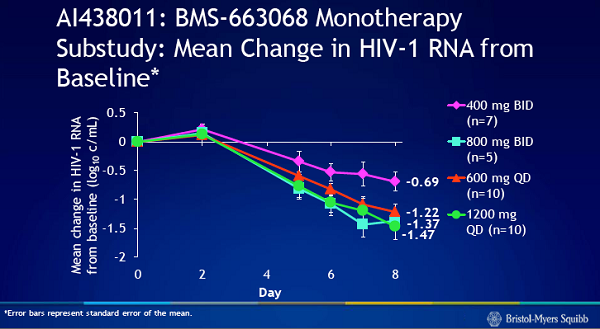
Uno studio proof of concept di 8 giorni in monoterapia ha fatto osservare delle riduzioni nella viremia da 1,2 a 1,7 log.
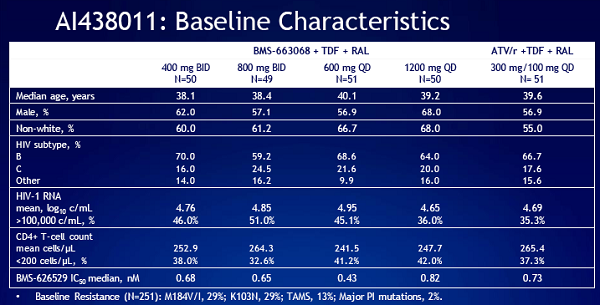
Lo studio presentato ora da Lalezari ha incluso 252 pazienti già trattati, con viremie di almeno 1000 copie/mL e più di 50 CD4. Nella slide che segue, tutte le caratteristiche di partenza: la maggior parte dei pazienti erano uomini, circa un terzo bianchi, l’età mediana era 39 anni. Due terzi dei partecipanti avevano un HIV di sottotipo B.
La media dei CD4 era di circa 230 cellule/mm^3 e circa il 40% ne aveva meno di 200. Molti avevano fallito dei regini di ART di prima e seconda linea. Circa la metà aveva almeno 1 mutazione importante, che li rendeva resistenti ad almeno una classe di antiretrovirali. Tutti potevano prendere raltegravir (Isentress), tenofovir (Viread) e atazanavir (Reyataz) e avevano dimostrato di essere sensibili al BMS-663068.
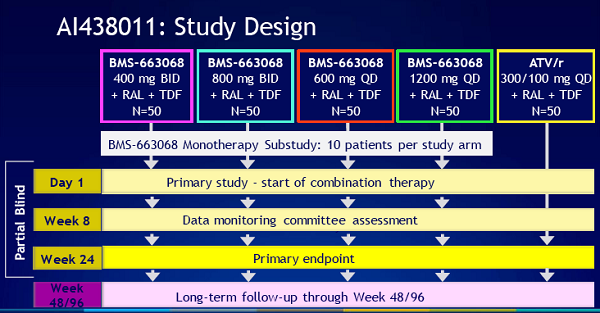
I partecipanti al trial sono stati divisi in modo casuale in 5 bracci: tutti hanno ricevuto tenofovir e raltegravir; il gruppo di controllo, in più, ha ricevuto atazanavir/ritonavir.
4 gruppi hanno ricevuto diversi dosaggi di BMS-663068 (400 o 800 mg due volte al giorno, 600 o 1200 mg una volta al giorno).
Nella diapositiva qui sotto si vedono anche i 32 pazienti che hanno seguito la monoterapia per una settimana.
Nel sottogruppo in monoterapia, si è visto un piccolo aumento dell’HIV RNA il secondo giorno che, a detta di Lalezari, potrebbe essere dipeso dal virus che, incapace di entrare nelle cellule, si è accumulato nel plasma.
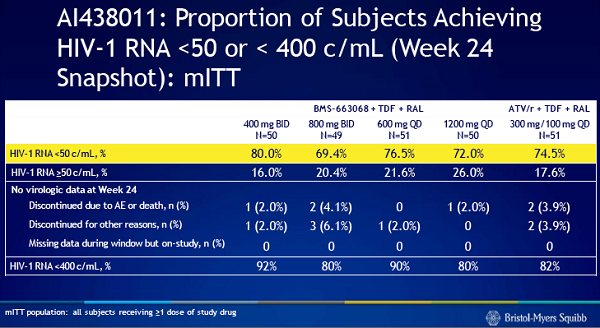
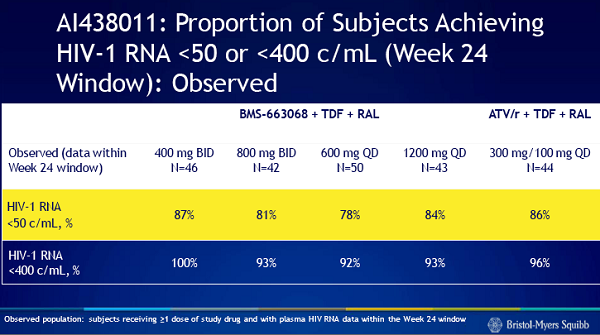
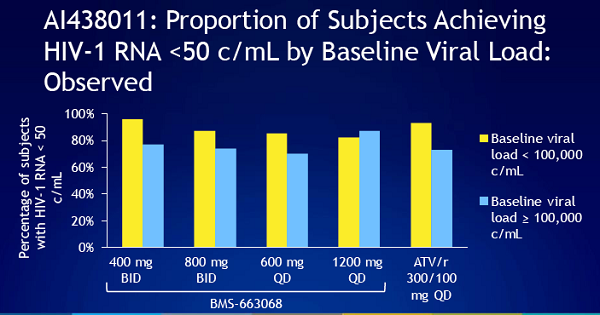
Dopo 24 settimane, tutti e 4 i bracci del trial hanno dimostrato un’efficacia simile nell’abbattere la viremia sotto le 50 copie: di chi aveva preso 400 mg due volte al giorno del farmaco, dopo 6 mesi l’80% aveva raggiunto viremia irrilevabile; di chi 800 mg due volte al giorno, il 69%; di chi 600 mg una volta al giorno, il 77%; e di chi 1200 mg una volta al giorno, il 75%.
Anche il guadagno in termini di CD4 è stato analogo nei 4 bracci:
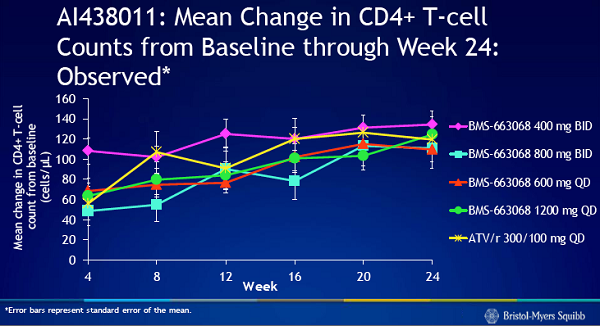
In generale, BMS-663068 è stato ben tollerato a tutti i dosaggi e Lalezari non ha segnalato problemi di sicurezza.
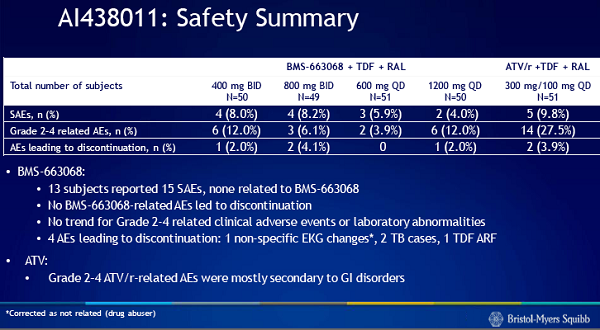
Conclusione: questi risultati suggeriscono che BMS-663068 sia efficace quanto uno dei regimi terapeutici standard, quindi inducono BMS a continuare nello sviluppo del farmaco.