Riprendo un post del 24 marzo dell'anno scorso per seguire in un nuovo thread un filone delle ricerche di Robert Siliciano che in questi giorni vede la pubblicazione di una nuova appassionantissima puntata: si tratta del tentativo di dar conto di quello sfasamento osservato fra l’effetto delle sostanze anti-latenza nei modelli cellulari in vitro e nei CD4 quiescenti prelevati ex vivo a persone con HIV in terapia soppressiva e la conseguente ipotesi che questi farmaci possano funzionare meglio se usati in combinazione.
Le immagini possono essere viste nel post originale, mentre la traduzione di un articolo della giornalista scientifica Alla Katsnelson sulla necessità di ripensare le strategie anti-latenza, scritto nel giugno scorso su Nature Reviews - Drug Discovery, segue subito sotto.
Dora ha scritto:In questi anni abbiamo visto fallire tutti i trial clinici “proof of concept” fatti per sperimentare qualche farmaco anti-latenza: lasciando perdere il debolissimo acido valproico, hanno fatto o stanno facendo una brutta fine il disulfiram, il vorinostat e il panobinostat – uno apparentemente più potente dell’altro. E anche le prospettive della romidepsina non si può dire che siano rosee, mentre di briostatina e prostratina in fase clinica dubito che sentiremo parlare in tempi ragionevoli.
Da profana, mi sono chiesta: perché tutte queste sostanze, che in vitro sembrano funzionare bene o addirittura benissimo e delle quali si sono misurate le diverse capacità di riattivare il virus latente (senza al tempo stesso attivare in massa tutti i CD4) in modo così preciso da poterle mettere in scala di potenza, quando finalmente vengono sperimentate in vivo, sembra che al virus che dorme non riescano a fare neppure il solletico?
Che cosa non funziona nei diversi modelli cellulari perché si rivelino così poco affidabili nel predire che cosa accadrà davvero nel corpo dei pazienti?
E in particolare: perché nei modelli riesci a stabilire che una sostanza è più potente di un’altra nel forzare la trascrizione del virus, e anche di quanto è più potente, e invece i risultati delle sperimentazioni cliniche sono molto simili (e vicini allo zero) per le diverse sostanze?
In questi anni, mi è capitato di leggere decine di lavori in cui si lamentava il fatto che nessun modello cellulare della latenza riesce da solo a catturare l’estrema complessità della realtà. Parallelamente, in ogni articolo, in ogni presentazione a un congresso, c’è sempre qualche ricercatore che sottolinea quanto sia difficile misurare correttamente il reservoir - una valutazione da cui non si può prescindere se si vuole capire se i farmaci antilatenza stanno avendo qualche effetto oppure no.
E già l’anno scorso, nell’ultima ricerca di cui abbiamo parlato in questo thread, dal laboratorio di Siliciano era venuta la dimostrazione che quello che è considerato il gold standard per misurare le dimensioni del reservoir latente – il Quantitative Viral Outgrowth Assay (QVOA) – non riesce a individuare la presenza di genomi provirali dopo che questi sono stati riattivati in vitro, mentre la PCR riesce ad amplificare un certo numero di “provirus non indotti” - tanto che Margolis - non ricordo più in quale occasione recente - ammise che, finché non si trova un modo per valutare davvero le dimensioni del reservoir, ogni trial clinico rischia di essere una semplice presa in giro.
Prima di arrivare alla sperimentazione in vivo, mancava inoltre un approfondito passaggio dai modelli in vitro alle cellule prelevate ex vivo da pazienti con viremia soppressa dalla terapia.
Questo passaggio l’ha fatto adesso Siliciano e qualche risposta comincia ad arrivare.
La ricerca è stata presentata al CROI tre settimane fa, ma ieri è uscito il relativo articolo su Nature Medicine, quindi metterò insieme qualche diapositiva della presentazione di Gregory Laird con quel che io ho recepito dell’articolo molto tecnico di Siliciano.
Detto molto brutalmente: nessuno dei farmaci antilatenza (latency-reversing agents – LRAs) sperimentati finora ha dimostrato di saper ridurre le dimensioni del reservoir latente in persone con HIV.
Il trattamento ex vivo con vorinostat di cellule di persone infette ha indotto, in certi studi, uno certo riattivarsi del virus, mentre in altri studi non si è visto neppure quello. Ma in vivo di produzione virale non se ne è vista.
Mancava finora una strategia validata ex vivo di confronto fra le diverse sostanze antilatenza, ed è quello che ha fatto Siliciano in questa ricerca, cercando di indurre la trascrizione virale in circa 5 milioni di CD4 quiescenti con vari LRAs e utilizzando tre test differenti per misurarne gli effetti. I test sono stati:
- 1. l’induzione di produzione virale – a indicazione di un’avvenuta inversione della latenza (Viral Outgrowth Assay – un tipo di test creato e ora modificato nel laboratorio di Siliciano);
2. il rilascio di virus libero fuori dalle cellule;
3. la produzione di HIV-1 mRNA intracellulare. È il metodo più comune per misurare mediante PCR l’induzione della trascrizione dell’HIV e consiste nella misura degli RNA che contengono sequenze della proteina Gag dell’HIV. Il problema - come viene dimostrato nell'articolo - è che anche se sono stati documentati aumenti di HIV-1 mRNA nei trial sul vorinostat di Margolis e di Lewin, questo metodo di misurazione non è del tutto affidabile, perché l'HIV mRNA può essere generato come risultato della trascrizione di geni umani entro i quali il virus si è integrato. Ma questo fenomeno non è la stessa cosa dell'attivazione del virus e non porta alla replicazione dell'HIV e alla produzione di virioni, che è la ragione per cui si usano i farmaci antilatenza.
Nei modelli cellulari, vorinostat, romidepsina, panobinostat, disulfiram e briostatina-1, dati in concentrazioni clinicamente accettabili, avevano dimostrato di poter invertire efficacemente la latenza senza avere effetti tossici sui CD4 quiescenti.
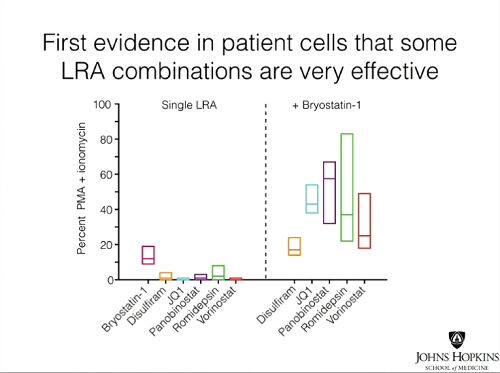
Le slides seguenti mostrano invece come da tutti e tre i tipi di test si sia visto che le singole sostanze anti-latenza non hanno causato produzione di virus nelle cellule prelevate dai pazienti con viremia soppressa dalla ART. Invece, trattando le cellule in coltura con PMA (forbolo miristato acetato) + ionomicina, un mix che causa attivazione cellulare e non può dunque essere usato nella clinica, tutte le cellule di tutti di pazienti hanno prodotto virus, che è stato possibile quantificare con un Viral Outgrowth Assay standard.
Le conclusioni dell’articolo:
Con questo l’articolo si chiude.
- I nostri dati dimostrano che nessuno dei principali candidati testati, fra le sostanze che invertono la latenza senza riattivare i linfociti T, è riuscito a distruggere in modo significativo ex vivo il reservoir latente. Il contrasto fra gli effetti dei LRAs nei modelli di latenza dell’HIV-1 in vitro e i loro effetti ex vivo nei CD4 quiescenti di persone infette in ART indica che questi modelli non catturano completamente tutti i meccanismi che governano la latenza dell’HIV-1 in vivo. È improbabile che queste sostanze portino all’eliminazione del reservoir latente in vivo quando somministrate individualmente.
L’unica sostanza efficace quando usata da sola è l’agonista della PKC [protein-chinasi C] briostatina-1, che probabilmente è troppo tossica per essere usata nella clinica.
Rimane da capire se altri agonisti della PKC o altre sostanze che stimolano meccanismi associati all’attivazione dei linfociti T possano essere abbastanza sicuri da essere somministrati ai pazienti ed è possibile che ulteriori progressi dipendano dal trovare delle combinazioni di LRAs che siano sicure e attive.
Invece, la lezione tenuta al CROI da Gregory Laird ci lascia con qualche speranza in più, perché ci mostra come alcune combinazioni di sostanze anti-latenza abbiano dimostrato di poter lavorare insieme, inducendo una maggior produzione di virus nelle cellule latentemente infette prelevate dai pazienti. Si è infatti osservato un potente ed efficace effetto sinergico quando sono stati uniti il panobinostat e soprattutto la romidepsina alla briostatina.
DdD: si sta preparando una terapia combinata anti-latenza, una specie di cALT?
FONTI:
- - Presentazione di Gregory Laird al CROI: Novel Ex Vivo Approaches Distinguish Effective and Ineffective Drugs for Reversing Latency In Vivo.
- Articolo su Nature Medicine: New ex vivo approaches distinguish effective and ineffective single agents for reversing HIV-1 latency in vivo.
- Comunicato stampa: Drugs fail to reawaken dormant HIV infection.
- Articolo del Siliciano Lab su PLoS Pathogens 2013 sulla validazione di un Rapid Viral Outgrowth Assay per misurare la frequenza di cellule che possono rilasciare virus capace di replicazione dopo essere state riattivate: Rapid Quantification of the Latent Reservoir for HIV-1 Using a Viral Outgrowth Assay.
- Articolo di Janet Siliciano e molti altri su PLoS Pathogens 2013 su uno studio comparativo di diversi test usati per misurare le dimensioni del reservoir: Comparative Analysis of Measures of Viral Reservoirs in HIV-1 Eradication Studies.
Dora ha scritto:Quando lo scorso marzo dal Siliciano Lab è arrivata la conferma di quanto si era osservato durante i trial clinici, e cioè che c’era uno sfasamento nell’effetto che le sostanze anti-latenza hanno nei modelli cellulari in vitro e quello che hanno ex vivo nei CD4 quiescenti di persone infette in terapia soppressiva, una nuova speranza veniva parallelamente offerta dalla possibilità di un uso congiunto di farmaci anti-latenza diversi.
Fu facile, allora, prevedere che stesse prendendo forma il concetto di terapia combinata anti-latenza e immaginare che potesse nascere l’acronimo cALT = combined Anti-Latency Therapy/Treatment.
Su Nature Reviews - Drug Discovery, la giornalista scientifica Alla Katsnelson ha pubblicato pochi giorni fa un breve articolo – Setback prompts rethink of latency-reversing strategy to eliminate HIV infection - che fa il punto della situazione sulle sperimentazioni fatte finora sui farmaci anti-latenza. È un lavoro semplice e molto chiaro, che mi sembra valga la pena tradurre per avere una visione di sintesi su alcune delle ricerche che stiamo seguendo in questa sezione del forum – e anche perché conferma che l’idea della cALT sta davvero prendendo consistenza.
Una battuta d’arresto spinge a ripensare alla strategia di inversione della latenza per eliminare l’infezione da HIV
I risultati contrastanti della prima generazione di sostanze che colpiscono l’infezione latente da HIV portano gli esperti a considerare combinazioni terapeutiche e nuovi test
I farmaci antiretrovirali sono stati efficaci in modo spettacolare nel controllare l’HIV ostacolando la capacità del virus di infettare le cellule, ma non distruggono i reservoir di cellule latentemente infette, che rimangono il principale ostacolo alla cura.
Una soluzione attraente a questo problema è stata quella delle sostanze che invertono la latenza (Latency Reversing Agents – LRAs), capaci di riattivare il virus dormiente, stanandolo dal suo nascondiglio in modo che possa essere colpito e ucciso.
Tuttavia, la prima generazione di LRA è di recente incappata in qualche difficoltà.
Uno studio ha dimostrato che quattro delle sostanze considerate migliori, che avevano mostrato delle potenzialità nei modelli di colture cellulari e negli studi clinici preliminari, hanno efficacia minima sulle cellule prelevate dai pazienti (Nature Med. 20, 425–429; 2014). Una quinta sostanza, per quanto più potente, è probabilmente troppo tossica per poter essere utilizzata in clinica.
Per molti che lavorano in questo campo, questi e altri dati indicano la necessità di un approccio “shock and kill” combinato, così come dello sviluppo di farmaci migliori. Ma i dati clinici potrebbero ancora salvare l’approccio con una singola sostanza. “Non sono del tutto convinto che questi test ex vivo colgano in pieno l’effetto dei farmaci in vivo” – dice Thomas Rasmussen, dell’università danese di Aarhus. “C’è un altro tipo di test che ci sta portando a una conclusione che non è necessariamente la medesima cui stanno arrivando altri laboratori”.
Il primo attacco in vivo all’approccio dei LRA venne una decina d’annoi fa, quando David Margolis, ora alla University of North Carolina, e colleghi trattarono quattro pazienti con acido valproico, un inibitore dell’iston-deacetilasi (Lancet 366, 549–555; 2005). Questi risultati – interessanti, ma preliminari – non furono confermati in sperimentazioni successive, ma diedero impulso a un impegno più ampio verso l’identificazione di nuovi LRA.
Per esempio, nel 2012 Margolis e colleghi pubblicarono uno studio molto stimolante, in cui si mostrava che il vorinostat, un altro inibitore dell’iston-deacetilasi, aumentava l’espressione dell’HIV RNA nei CD4 quiescenti in otto pazienti (Nature 487, 482–485; 2012).
Tuttavia, nonostante dati incoraggianti su diversi HDACi e altre piccole molecole nei modelli in vitro – compresa una positiva attività della romidepsina su cellule tratte da pazienti riferita lo scorso aprile (PLOS Pathog., 10 Apr 2014) – i dati clinici che ne sono seguiti sono stati contrastanti.
In una ricerca recente, Robert Siliciano e colleghi della Johns Hopkins University School of Medicine, Maryland, si erano prefissi di studiare gli effetti del disulfiram su 16 persone con HIV. il disulfiram, che è usato per trattare l’alcolismo, aveva mostrato una certa attività in un modello cellulare, ma non ha avuto alcuna efficacia nel trial clinico pilota (Clin. Infect. Dis. 58, 883–890; 2014). “Questo è proprio quello che ci ha spinto a dire ‘OK, dobbiamo tornare indietro e vedere se questi modelli ci dicono davvero quello che accade nelle cellule dei pazienti” – dice Siliciano.
Nei test basati su cellule tratte dai pazienti che hanno sviluppato, come riferito nel recente articolo su Nature Medicine, né i tre HDACi che hanno testato – vorinostat, panobinostat e romidepsina – né altre due sostanze – il disulfiram e la briostatina-1 – hanno indotto produzione virale, il gold-standard per misurare la riduzione della latenza.
Tutti, tranne la briostatina-1, hanno indotto solo un piccolo aumento dei livelli di HIV mRNA nelle cellule tratte da 13 persone con HIV. “Se l’attivazione dei linfociti T causa un aumento di 100 volte nell’HIV mRNA, queste sostanze possono causare un aumento di 2 volte” – dice Siliciano.
La briostatina-1 ha prodotto un aumento da 3 a 5 volte nei livelli di mRNA, ma ha anche causato una significativa tossicità alle cellule. “Non è chiaro se questo farmaco sarà mai abbastanza sicuro da usare in questo contesto” – nota Siliciano.
Jerome Zach, direttore del Center for AIDS Research della University of California, Los Angeles, sta invece sviluppando degli analoghi di sintesi della briostatina-1 – chiamati “briologhi” – con l’obiettivo di minimizzarne la tossicità.
Combinazione di LRAs
“È possibile che questi farmaci funzionino se usati in qualche combinazione” – dice Siliciano. “È solo che, fino ad ora, presi singolarmente non sono stati particolarmente efficaci”. E questo non dovrebbe sorprendere – aggiunge: la terapia combinata è stata storicamente la strada da percorrere con l’HIV. Il suo gruppo ha già iniziato a testare combinazioni di sostanze nei modelli costruiti con cellule prese dallo stesso paziente, anche se è un processo molto macchinoso – dice.
La Merck sta utilizzando screening detti “ad alto rendimento” per identificare combinazioni di LRA – dice Daria Hazuda, capo delle ricerche per le malattie infettive ai Laboratori di ricerca Merck. L’espressione del virus latente è modulata dalla cromatina, e ciò la rende suscettibile di essere colpita dagli HDACi, ma viene anche ristretta attraverso altri meccanismi al livello della trascrizione e forse anche della traduzione, quindi colpire una combinazione di meccanismi potrebbe produrre i risultati migliori. “Stiamo iniziando a raccogliere alcune idee interessanti su come ottimizzare delle combinazioni in modo più sistematico e razionale” – dice.
Anche una manciata di altre società, compresa Gilead Sciences, stanno lavorando in questo campo – aggiunge.
Studi su scimmie infettate dal virus dell’immunodeficienza scimmiesca (SIV) e su topi umanizzati saranno cruciali per capire come i LRA lavorino in vivo – dice Margolis. Ci sono in corso degli studi su una combinazione di vorinostat e prostratina, così come su altri HDAC, agonisti della protein-chinasi C (PKC), inibitori del bromodomain e altri composti come l’ingenol, testati da soli o in combinazione. “Degli studi di combinazione su esseri umani, a mio parere, non sono ancora sicuri” – aggiunge.
Invece, Rasmussen continua a sperare in sostanze singole. Al CROI lo scorso marzo ha riferito che il panobinostat – uno dei farmaci che hanno mostrato una attività minima nel recente studio di Siliciano – ha indotto un aumento nei livelli di HIV mRNA associati alle cellule e nel plasma in un trial su 15 pazienti (CROI Poster Abstract 438LB).
“Noi pensiamo che questo composto sia in grado di attivare la produzione di virus in misura tale che effettivamente si producano particelle virali, che vengano poi rilasciate nel flusso sanguigno” – sostiene Rasmussen.
Altri trial su singoli LRA sono ancora in atto. Ricercatori australiani hanno riferito al CROI nel 2013 che il vorinostat aveva stimolato i livelli di mRNA associato alle cellule in 18 pazienti su 20, e anche il team di Margolis sta conducendo dei trial di follow-up degli studi clinici sul vorinostat. All’inizio di quest’anno, poi, è partito un trial sulla romidepsina condotto dall’AIDS Clinical Trials Group.
Anche Rasmussen e colleghi hanno di recente iniziato un trial sulla romidepsina somministrata insieme a un vaccino terapeutico, con l’idea di stimolare le risposte dei CD8 contro il virus riattivato.
Servono più test
Le scoperte fatte ultimamente da Siliciano mettono in evidenza la necessità di modelli migliori, che facciano migliori predizioni rispetto ai modelli usati fino ad oggi – aggiunge Werner Greene, un ricercatore della University of California, San Francisco. “Quello di cui abbiamo bisogno è una popolazione di cellule tratte dai pazienti che siano molto più pure ed omogenee rispetto a quelle che possiamo avere in numero illimitato” – dice, osservando che lui stesso sta collaborando allo sviluppo di tali cellule, mediante l’utilizzo di una tecnologia che permette di indurre cellule staminali pluripotenti.
Hazuda concorda sul fatto che testare i farmaci su cellule tratte da pazienti è importante, ma invita alla cautela, poiché non è ancora sicuro che i test sulle cellule dei pazienti siano migliori di altri tipi di esperimenti. “Finché non otterremo davvero dati in vivo per costruire dei modelli standardizzati sarà difficile dire che un test è più utile o fa predizioni migliori di un altro” – dice.
Ci sono diverse altre questioni ancora da risolvere. Per esempio, non è chiaro quanto virus sia necessario riattivare. “La misurazione importante, probabilmente, è quanto antigene viene esposto dalla cellula infetta “ – dice Margolis. “cioè, la cellula può essere identificata e distrutta?” Anche questo rende difficile valutare funzionalmente le risposte ai LRA.
Un’altra questione, poi, è che sia i modelli in vitro, sia i test ex vivo derivati dai pazienti come quello di Siliciano, usano linfociti T quiescenti circolanti. Ma le cellule latenti si ritiene stiano prevalentemente nei tessuti, come l’intestino e il sistema nervoso centrale, ed è possibile che queste cellule rispondano ai farmaci in modo diverso.
Può anche essere difficile trovare un equilibrio fra la riattivazione del virus e l’attivazione dei linfociti T, che inverte la latenza, ma può scatenare una tempesta di citochine. “Questa biologia del virus è così inestricabilmente legata all’attivazione dei linfociti T, che rischia di essere difficile trovare sostanze che stimolino l’espressione del virus senza però attivare la cellula” – dice Greene.
Nonostante tutto questo, i ricercatori sono ottimisti sul fatto che l’approccio con i farmaci anti-latenza possa funzionare. “Dobbiamo essere realisti e guardare al progresso che abbiamo fatto con un investimento che – relativamente parlando – non è stato enorme” – dice Margolis. “Questo campo di ricerca sta solo iniziando a muoversi”.
Continua nel prossimo post.





