A questa domanda ieri Uffa ha risposto: "gli antiretrovirali non sono mai troppi" - così ho deciso, complice il fatto che un paio di settimane fa al CROI Merck ha annunciato di essere pronta a dare inizio alla fase III di sperimentazione, di dedicare un thread tutto suo alla DORAVIRINA (un tempo MK-1439).
Ma la vera ragione che mi ha spinto a parlarne è che
- DORAvirina batte
UFFAefavirenz (almeno) 3 a 0.
- - migliore capacità di soppressione delle viremie,
- maggior recupero immunologico,
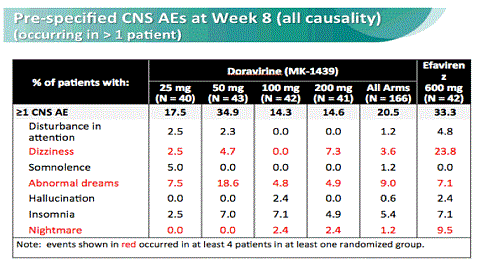
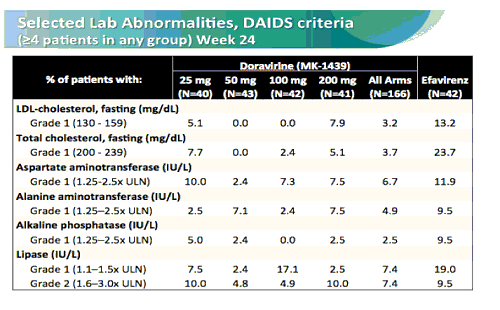
- minore tossicità (soprattutto a livello epatico), niente incubi, né allucinazioni.
Andiamo per ordine.
Prima un post preparato per il CROI dell'anno scorso.
Da [CROI 2013] I nuovi farmaci
Dora ha scritto:Ed ora ... ECCO A VOI LA DORAVIRINA!
CROI 2013: MK-1439, a Novel HIV NNRTI, Shows Promise in Early Clinical Trials
Published on Wednesday, 06 March 2013 00:00 Written by Liz Highleyman
Un inibitore non-nucleosidico della trascrittasi inversa (NNRTI) di nuova generazione – l’MK-1439 – ha dimostrato una forte attività antiretrovirale e una buona tollerabilità in monoterapia in un piccolo studio clinico – hanno raccontato i ricercatori il 5 marzo al CROI.
Gli NNRTI sono in genere ben tollerati e sono adatti ai trattamenti di prima linea dell’HIV, ma costituiscono una classe di farmaci che crea facilmente resistenze. Gli studi preclinici hanno dimostrato che l’MK-1439 ha un’elevata attività contro ceppi dell’HIV che hanno delle mutazioni resistenti ad altri diffusi NNRTI (comprese la K103N e la Y181C). A differenza di un NNRTI molto usato come l’efavirenz (Sustiva), sembra avere scarso potenziale tossico nei confronti del sistema nervoso centrale.
Matt Anderson, della Merck, e colleghi hanno analizzato l’MK-1439 in un trial in doppio cieco, controllato con placebo, in un unico sito a Berlino. I ricercatori hanno valutato sicurezza, tollerabilità, attività antivirale e farmacocinetica del farmaco, nonché la resistenza virale durante la somministrazione di dosi multiple.
Questo studio è stato il primo a testare le dosi multiple di MK-1439 in persone con HIV. La ricerca precedente aveva dimostrato una sicurezza e una farmacocinetica accettabili in volontari HIV negativi, cui era stata data una singola dose fino a 1200 mg (vedere poster 527).
Questa analisi ha incluso 18 persone con HIV mai trattate. Anche se sia gli uomini, sia le donne, sono stati arruolati nel trial solo degli uomini, di età fra i 25 e i 45 anni, con almeno 200 CD4/mm3 all’ingresso nello studio e valori biochimici ed ematologici normali. Le persone con co-infezione con epatite B o C sono state escluse.
I partecipanti sono stati randomizzati per ricevere 25 o 200 mg una volta al giorno di MK-1439, oppure placebo, come monoterapia per 7 giorni. Dopo il completamento del dosaggio, i partecipanti hanno iniziato una terapia antiretrovirale combinata standard per altri 10 giorni, in modo da evitare che l’MK-1439 residuo potesse causare lo sviluppo di resistenze in assenza di altri antiretrovirali.
Risultati
“L’MK-1439 è stato in genere ben tollerato, senza tendenze significative da un punto di vista clinico o segnali evidenti nei marker vitali, nei valori biochimici o nell’ECG”, hanno concluso i ricercatori. “Si è vista una robusta attività antivirale contro l’HIV-1 sia con la dose giornaliera di 25 mg, sia con quella di 200.”
- • L’MK-1439 ha dimostrato una potente attività antivirale.
• I livelli di viremia sono crollati regolarmente per le persone che prendevano entrambi i dosaggi di MK-1439, mentre sono rimasti stabili in chi prendeva il placebo.
• Il 7° giorno di trattamento, i declini dell’HIV RNA erano simili in chi prendeva 25 mg e in chi ne prendeva 200, rispettivamente a 1,37 e a 1,26 log.
• Nessun partecipante ha mostrato prove di comparsa di resistenze dopo 7 giorni di monoterapia.
• I parametri farmacocinetici dell’MK-1439 erano simili a quelli visti in precedenza nei volontari HIV negativi che avevano preso i medesimi dosaggi.
• I livelli del farmaco hanno raggiunto uno stato costante dopo 3 o 5 giorni e l’emivita media effettiva nel corpo è stata di 10-16 ore.
• L’MK-1439 ha continuato ad apparire sicuro e ben tollerato.
• Anche se circa di ¾ dei partecipanti hanno sperimentato eventi avversi, questi sono stati per lo più da lievi a moderati in intensità e si sono risolti dopo la fine del trattamento.
• Solo 3 eventi sono stati considerati potenzialmente connessi al farmaco (sudori notturni, mal di testa e perdita di appetito).
• L’univo evento avverso grave – un aumento degli enzimi epatici in una persona con epatite C acuta – è stato considerato probabilmente non correlato con il farmaco studiato.
• Ad oggi non sono stati riferiti rash cutanei significativi, eventi neurologici o anomalie nella biochimica.
Anderson ha detto che un trial clinico di fase IIb sta arruolando pazienti per confrontare l’MK-1439 con l’efavirenz, entrambi insieme a tenofovir/emtricitabina (i farmaci presenti nel Truvada). Maggiori dettagli sono disponibili in http://www.clinicaltrials.gov/ct2/show/NCT01632345.
Fonti
- M Anderson, J Gilmarti, M Robberechts, et al. Safety and Antiviral Activity of MK-1439, a Novel NNRTI, in Treatment-naive HIV+ Patients. 20th Conference on Retroviruses and Opportunistic Infections. Atlanta, March 3-6, 2013. Abstract 100.
- M Anderson, J Gilmarti1, M Robberechts, et al. Safety, Tolerability, and Pharmacokinetics of Single and Multiple Doses of MK-1439, a Novel HIV NNRTI, in Healthy Subjects. 20th Conference on Retroviruses and Opportunistic Infections. Atlanta, March 3-6, 2013. Abstract 527.
Ora il breve annuncio dei buoni risultati portati al CROI di quest'anno e in un prossimo post qualche dettaglio in più.
Dora ha scritto:Nei prossimi giorni spero di riuscire a preparare un thread a parte, dedicato ai nuovi farmaci di cui si è parlato al CROI 2014, ma non posso evitare di darne qui una anticipazione - per tutti i fan dellaDORAVIRINA
: pare che la fase IIb sia andata benissimo.
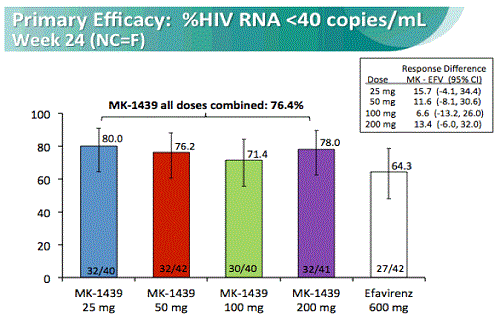
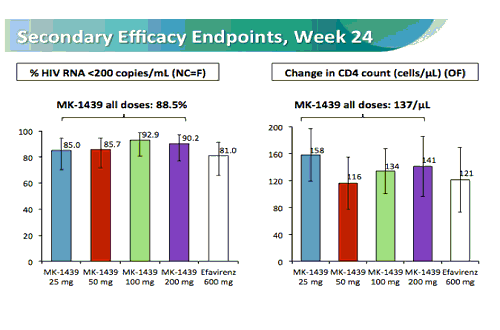
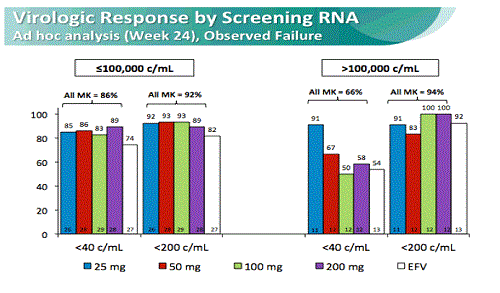
Si tratta di un trial randomizzato e in doppio cieco su sicurezza, tollerabilità ed efficacia di dosaggi variabili di doravirina somministrati una volta al giorno (25, 50, 100 e 200 mg) in combinazione con tenofovir/emtricitabina (Truvada) e confrontati con 600 mg al giorno di efavirenz.
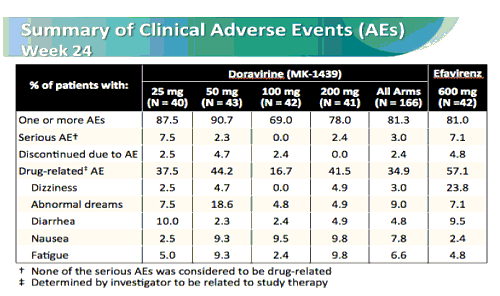
Eventi avversi sostanzialmente trascurabili.
Nella seconda metà del 2014 parte la fase III.