ADVANCES IN IMMUNOLOGY
Trkola esordisce con uno dei leitmotiv che più stanno segnando la ricerca su HIV in questi anni: si deve iniziare presto - qualunque cosa sia, scoprire l'infezione, iniziare la terapia antiretrovirale o fare un qualsiasi tentativo di curare l'infezione, prima si parte e meglio è.

E se è vero il detto che "il primo uccello cattura il verme" [in italiano non suona tanto bene, mi spiace - noi usiamo piuttosto che "il mattino ha l'oro in bocca" o che "chi prima arriva meglio alloggia", ma così perdiamo la graziosa immagine proposta da Trkola e la sua affinità con la parte destra dell'immagine seguente]

questo a maggior ragione vale nel caso degli anticorpi neutralizzanti ad ampio spettro (bNAbs) di cui si parlerà in molte presentazioni al congresso. Ma ci sono anche tanti bei progressi nella ricerca sui linfociti T CD8 (a sinistra nella slide), che se attivati contro le cellule infette presto, nei primi tempi dell'infezione, lavorano molto meglio che dopo tanti anni di ART.
Trkola ricorda che la Bernard Fields Lecture, quest'anno tenuta da Julie Overbaugh, sarà dedicata ai primi eventi subito dopo la trasmissione dell'infezione da mamma a bambino e al ruolo dei bNAbs in queste primissime fasi dell'infezione. Ci sarà poi un intero simposio per discutere degli interventi da fare per colpire queste fasi precoci (""STOP IT NOW: TARGETING EARLY INFECTION EVENTS).
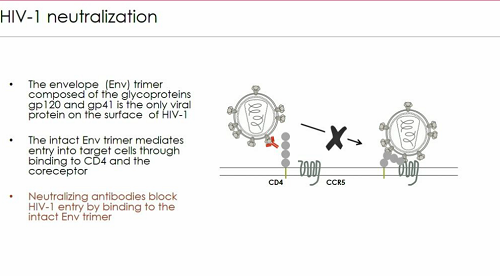
Passando alla questione della neutralizzazione di HIV, Trkola ricorda che il trimer della envelope di HIV è l'unica proteina esposta sulla superficie del virus ed è composto da due glicoproteine, gp120 e gp41. Quando è intatto, media l'ingresso del virus nella cellula legandosi al CD4 e al CCR5 (o al CXCR4). La funzione degli anticorpi neutralizzanti,la loro attività inibitoria, è dunque quella di impedire ad HIV l'ingresso legandosi al trimer della Env.
In tutte le persone con HIV si verifica un'evoluzione delle risposte neutralizzanti, che si rivela prevalentemente specifica per determinati ceppi virali autologhi (ciòè presenti in quel particolare individuo). HIV, però, è capace di modificare la Env in modo da sfuggire all'azione neutralizzante degli anticorpi. E lo fa più velocemente di quanto gli anticorpi riescano ad adattarsi, è sempre un passo avanti a loro.
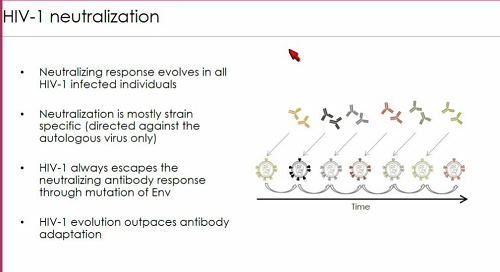
Nell'infezione non trattata, l'interazione fra virus, mutazioni di escape e adattamento degli anticorpi può andare avanti per anni e porta ad un aumento della diversità della Env, a un'esposizione prolungata agli antigeni di Env del sistema immunitario e, quindi, a un aumento della capacità di neutralizzazione degli anticorpi e dell'ampiezza di questa risposta, che riesce a dirigersi contro un numero sempre maggiore di proteine Env mutate.
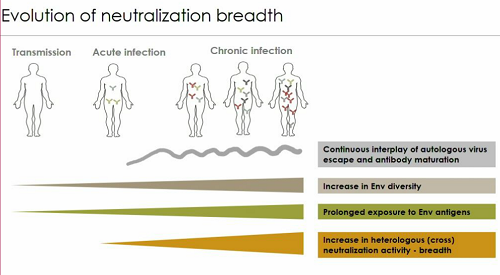
Questo porta, in alcuni pazienti, alla formazione di bNABs, anticorpi che sono capaci di distruggere un gran numero di varianti virali, che sono molto potenti e che sia in vitro, sia in vivo nei modelli animali hanno dimostrato di esercitare un certo grado di protezione.
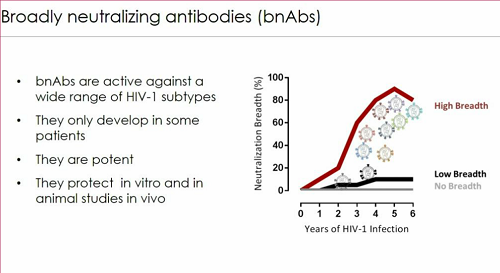
La scoperta dei bNAbs non si è ancora tradotta nella nostra capacità di indurre la loro produzione mediante un vaccino - però questa è una delle strade che la ricerca sta seguendo. Le altre due strade seguite sono quella di usare i bNABs come prevenzione attraverso l'immunizzazione passiva (cioè somministrandoli dall'esterno, come nello studio AMP, che si sta già svolgendo sull'uomo) e di usarli in funzione terapeutica, per ritardare e ridurre il rebound delle viremie se si interrompe la ART (e ci sono almeno un paio di studi su animali che stanno andando bene).
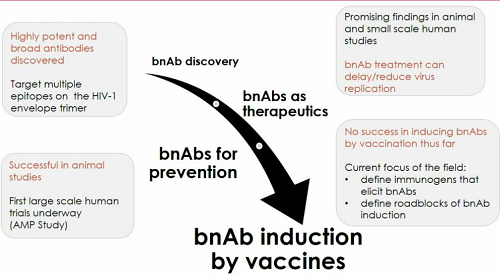
Gli studi principali che si stanno svolgendo sui bNABs riguardano, oltre alla scoperta e alla caratterizzazione di sempre nuovi anticorpi, alla comprensione di come questi effettivamente interagiscano con il virus, come si evolvano nel paziente e come possano essere indotti in vivo, anche la costruzione di vaccini, disegnando la parte immunogenica del vaccino, che è quella che deve indurre il sistema immunitario a produrre i bNAbs, e definendo i correlati di protezione.
La parte destra della slide che segue illustra i modi diversi con cui si intendono utilizzare questi anticorpi.
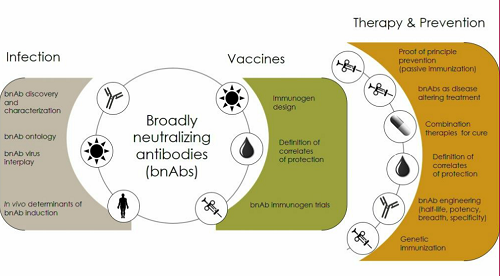
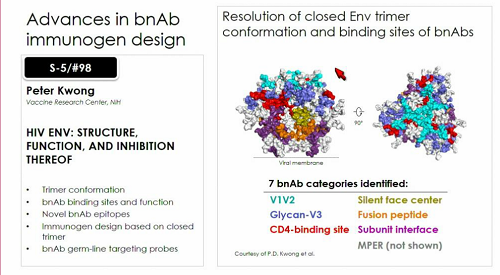
Trkola illustra poi brevemente la presentazione che Peter Wong terrà sulla struttura e la funzione della Env e su come inibirla.
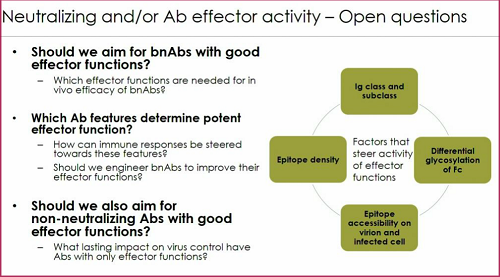
La slide che segue illustra le questioni ancora aperte relativamente all'uso dei bNAbs nella prevenzione: possono davvero proteggere? quanti ce ne vogliono perché si sia protetti dal contagio? in che modo davvero agiscono? neutralizzano soltanto il virus, oppure riescono anche a inibirne la trasmissione da cellula a cellula? oltre a una attività neutralizzante, ne hanno anche una effettrice?

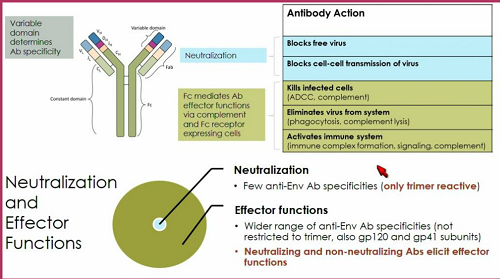
La porzione variabile (le parti colorate nei due rami della Y nella slide qui sotto) determina la specificità dell'anticorpo; la porzione costante, invece, (in verde) media la funzione effettrice dell'anticorpo.
Nella parte a destra della diapositiva sono elencate le attività degli anticorpi anti-HIV: in azzurro quelle connesse alla neutralizzazione, in verde le attività mediate dall'attività effettrice.
In basso, Trkola descrive quello che possiamo attenderci dai bNABs contro HIV che abbiamo oggi a disposizione: una piccola frazione di attività neutralizzante, perché gli anticorpi possono legarsi soltanto a un trimer di Env che sia intatto; una maggior frazione di attività effettrice.
Seguono le questioni aperte riguardo all'attività neutralizzante e/o effettrice dei bNAbs (sulla seconda, ci sono almeno una decina di abstract).
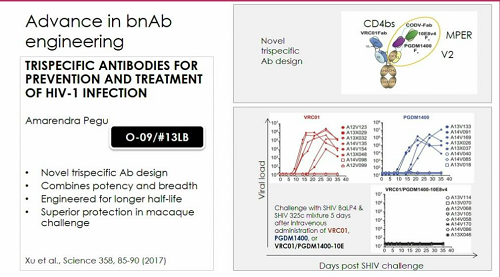
Sulla costruzione di anticorpi sempre più complessi ed efficaci (ora siamo arrivati, dopo i bi-bNABs, ad avere dei BnAbs TRIspecifici), Trkola annuncia la lezione di Amarenda Pegu:
Per la prevenzione mediante bNABs, la parte del leone la fa ovviamente lo studio AMP, perché è già in atto ed è ampio, impostato su più coorti che hanno arruolato persone con esigenze assai diverse.

Gli obiettivi che un intervento con bNABs si può porre in campo terapeutico sono elencati nella slide che segue. In fondo a destra quello che i primi studi sugli animali e i pochi studi su esseri umani stanno cominciando a insegnarci: è possibile ritardare il rebound delle viremie, è possibile abbassarne il set point, è possibile mantenere la soppressione della viremia per tempi più o meno lunghi.
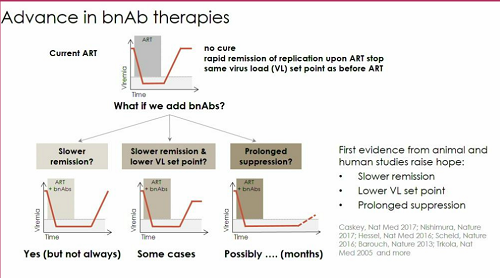
Restano, ovviamente, ancora tante cose da capire: come risolvere il problema delle varianti di escape, che sono sorte in ogni studio e hanno quasi sempre vanificato l'efficacia dell'anticorpo? in quali casi i bNABs possono essere più efficaci? che cosa si deve fare per aumentarne l'efficacia?

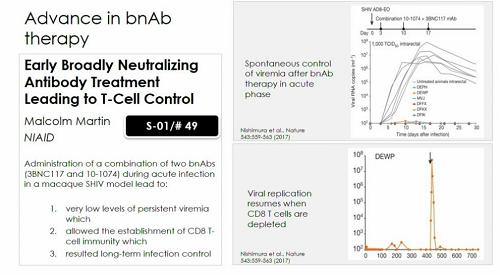
La somministrazione combinata di due bNAB (3BNC117 e 10 1074) a macachi in infezione acuta ha avuto ottimi risultati. Ce ne parlerà Malcom Martin. Ma gli abstract sui bNABs sono moltissimi.
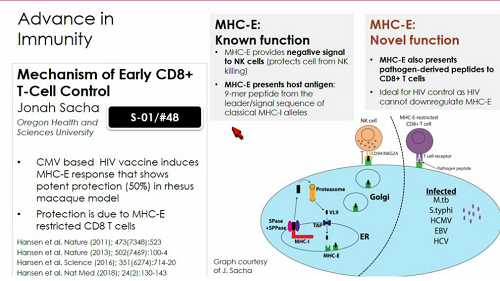
Trkola ricorda poi che si stanno facendo progressi anche nello studio dei CD8. Attesa la presentazione di Jonah Sacha, che lavora con Picker al vaccino basato sul CMV: sembra che stiano definendo meglio il tipo di risposte stimolate dal loro vaccino (anche se penso che dopo il CROI dell'anno scorso abbiano abbandonato le speranze di usarlo in funzione terapeutica)
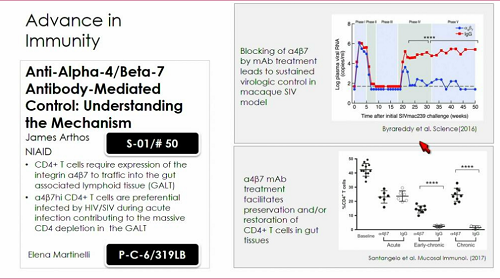
Infine il lavoro del NIAID sull'anticorpo α4β7, di cui stanno continuando a cercar di capire il meccanismo d'azione.