La lezione che Richard Koup, Vaccine Research Center, NIAID, ha tenuto ieri al Worshop for New Investigators ha toccato i temi dell’immunologia e dei vaccini, a partire da alcune delle novità di questi ultimi tempi. In particolare, si è occupata di microbioma, anticorpi neutralizzanti ad ampio spettro (bNAbs) e di CD8.
Per essercene occupati a lungo trattando della truffa del GcMAF e dello yoghurt magico di Marco Ruggiero, sappiamo che parlare di microbioma va molto di moda ultimamente. Se molti ne parlano a vanvera e alcuni ciarlatani sfruttano la moda per vendere i loro intrugli, ci sono però anche molti scienziati seri che stanno cercando di definire il ruolo del microbioma sia negli stati di salute, sia in quelli di malattia. L’infezione da HIV non fa eccezione e anche qui le popolazioni di microbi che risiedono nel tratto gastrointestinale svolgono un ruolo.
Koup inizia dunque la sua lezione con una frase ad effetto, che poi si preoccuperà di motivare (e in parte anche di ridimensionare): IL MICROBIOMA TOCCA TUTTO!
Ed ecco in che senso:
- - sopra e dentro il corpo umano vivono più di 10^14 batteri, appartenenti a più di 1000 specie diverse (le cellule eucariote in un essere umano adulto sono circa 10^13, quindi si può sostenere che noi siamo più procarioti di quanto siamo eucarioti).
Nel microbioma intestinale umano troviamo tre gruppi principali:
- - i firmicutes sono per lo più Gram positivi, coinvolti nel riassorbimento dell’energia e nell’assorbimento degli acidi grassi (Clostridia, Bacillus, Streptococcus, Staphylococcus, Lactobacillus, Bifidobacteria);
- i batteroidi sono Gram negativi, anaerobici e riescono a processare delle molecole complesse trasformandole in molecole semplici (Bacteroides, Prevotella);
- i proteobacteria sono Gram negativi, talvolta anaerobici e molto spesso patogeni (Escherichia, Helicobacter, Yersinia, Pseudomonas).
Esistono molti microbiomi nel nostro corpo, anche se ci si concentra di solito sul microbioma intestinale, e specificamente su quello dell’intestino crasso e delle feci.
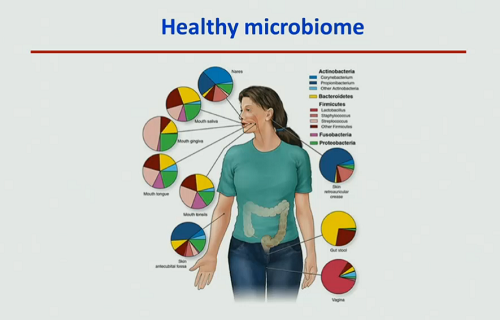
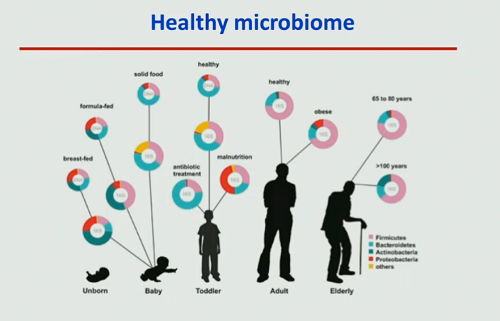
Il microbioma subisce modificazioni in funzione dell’età, dell’alimentazione, dell’assunzione di farmaci, del peso
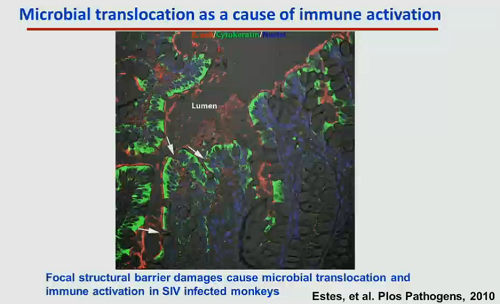
Nell’infezione da HIV, la traslocazione microbica è una delle principali cause di attivazione immunitaria, che è una delle complicanze maggiori. Nella slide qui sotto si vede l’intestino di una scimmia infetta da SIV: le frecce indicano i punti in cui la barriera è danneggiata e lascia passare batteri nel circolo sanguigno.
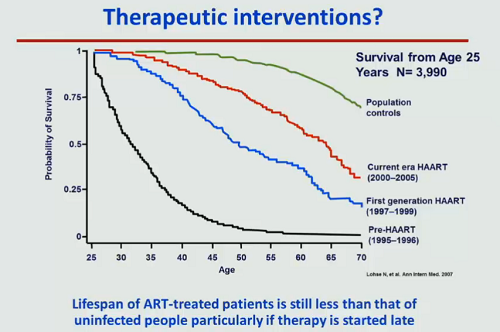
Nonostante la ART abbia enormemente ampliato le prospettive di vita delle persone con HIV, soprattutto in chi la comincia in una fase avanzata dell’infezione permane uno scarto rispetto all’aspettativa di vita delle persone senza HIV e questo scarto è da attribuire principalmente ai danni causati dall’immunoattivazione.
Negli ultimi anni, ricerche molto serie hanno confermato che nelle persone affette da HIV si riscontra disbiosi causata dall’alterazione della mucosa intestinale.
Il microbioma delle persone con HIV presenta delle differenze rispetto a quello delle persone HIV negative, con una diminuzione dei firmicute e un aumento di proteobatteri, che sono considerati infiammatori. Questo slittamento verso i proteobatteri si associa con l’aumento di diversi marker infiammatori, in particolare con l’attivazione dei CD8.
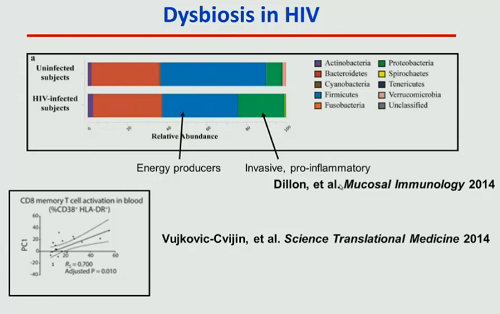
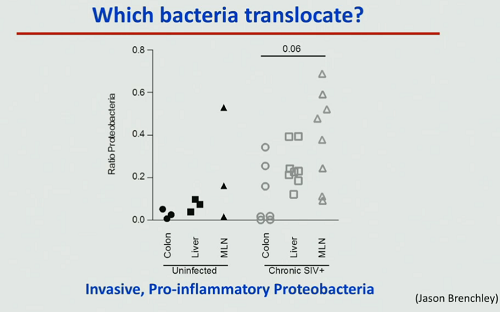
Non si ha solo un cambiamento del microbioma, ma anche un cambiamento del tipo di batteri che traslocano, con un aumento della traslocazione di batteri infiammatori.
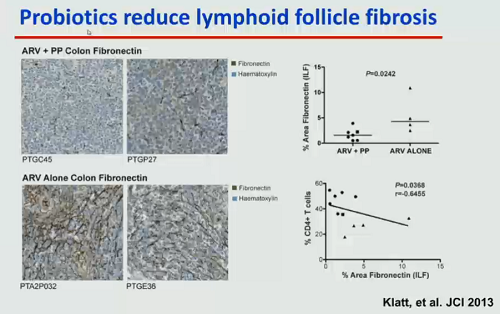
I probiotici un poco aiutano a ridurre la fibrosi del tessuto linfoide [però finora si è visto che miglioravano la mucosa intestinale delle scimmie trattate con antiretrovirali, mentre negli uomini facevano poco]
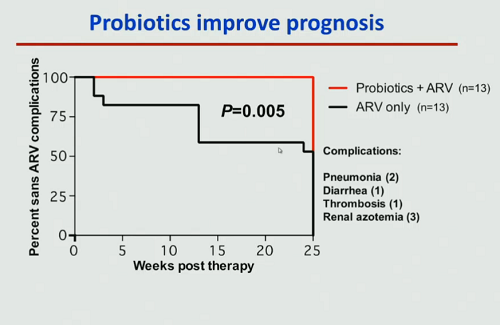
Quando le scimmie sono state seguite per un tempo più lungo, si è anche visto che la somministrazione di probiotici migliorava la prognosi e soffrivano di un minor numero di complicazioni. L’immunoattivazione, però, non veniva completamente meno.
Koup passa poi alla questione della possibile influenza del microbioma sull’efficacia dei vaccini, ricordando due vaccini – quello Thai (RV144) e uno che usava come vettore l’Adenovirus 5 (HVTN 505): il primo dimostrò di dare qualche protezione, il secondo fallì miseramente un paio d'anni fa.
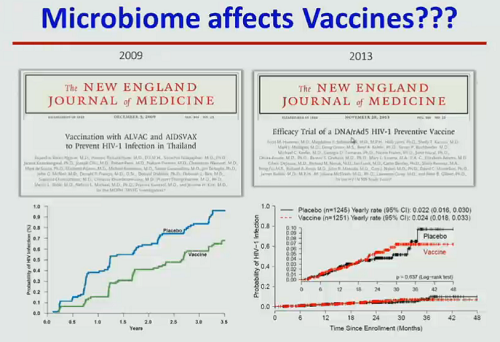
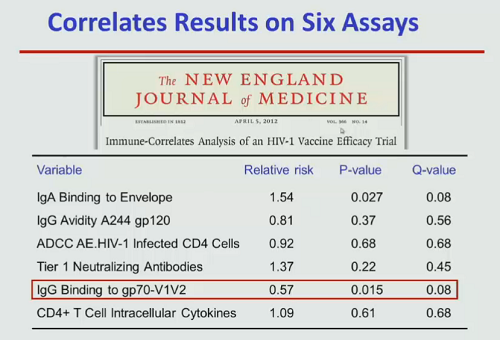
Quando si sono indagate le ragioni per cui il vaccino Thai era riuscito a dare una qualche protezione contro l’infezione, si è visto che uno dei maggiori correlati di protezione è stata la capacità del vaccino di creare anticorpi che si legavano al dominio V1 V2 della glicoproteina gp70 (cioè la Env).
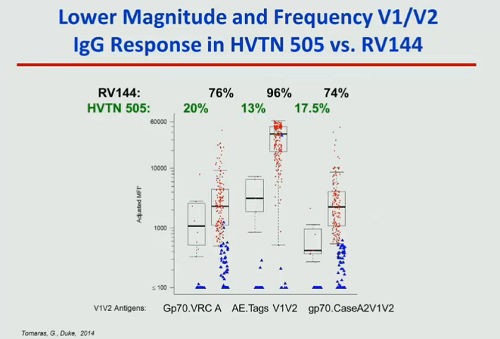
Confrontando la risposta anticorpale nel caso dei due vaccini, RV144 e HVTN 505, si è visto che nel caso del vaccino Thai la produzione di anticorpi era di gran lunga maggiore.
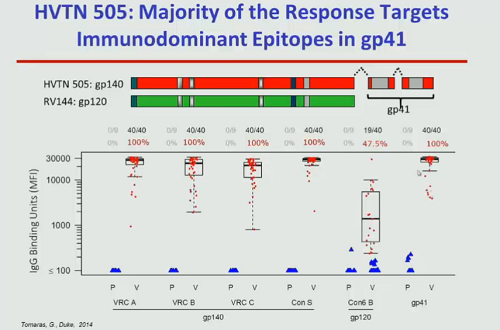
La ragione è stata individuata nel fatto che nell’HVTN 505 la maggioranza delle risposte colpiva epitopi nella glicoproteina gp41 (che era inclusa fra gli immunogeni del vaccino fallito, mentre era assente dal vaccino Thai). Così nel vaccino HVTN 505 non si sono quasi sviluppate risposte alla gp120, mentre quasi tutte le risposte erano dirette contro la gp140.
Un lavoro pubblicato l’anno scorso dal gruppo di ricerca di Barton Haynes alla Duke University ha dimostrato che c’era stata una reazione crociata fra anticorpi diretti contro la gp41 e il microbiota. Molte persone hanno nel loro repertorio di linfociti B hanno dei linfociti B che esprimono degli anticorpi che si indirizzano contro il microbiota e hanno reagito in modo incrociato contro la gp41. Quando sono stati immunizzati con un vaccino che conteneva la gp41, si sono avuti tanti anticorpi che reagivano contro questa proteina e quasi nessuno che si indirizzasse contro V1 V2 o gp120.
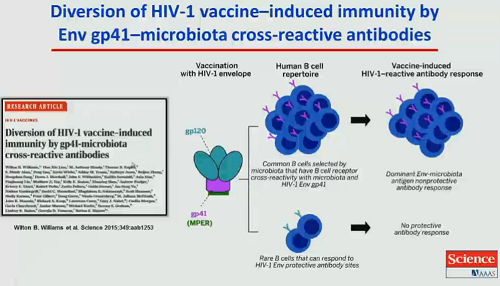
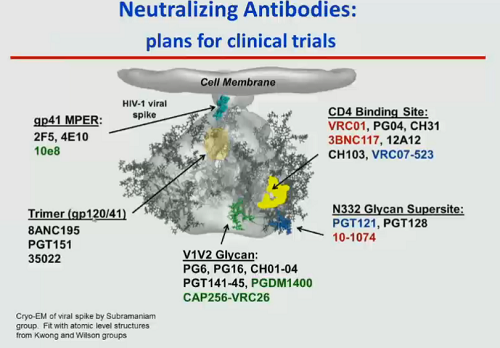
Passando a parlare di bNAbs, Koup si chiede se siano dei nuovi farmaci miracolosi, mostra dove alcuni bNAbs si aggancino in diverse regioni degli spike sulla Env dell’HIV e ricorda come alcuni di questi anticorpi siano già studiati in sperimentazioni cliniche.
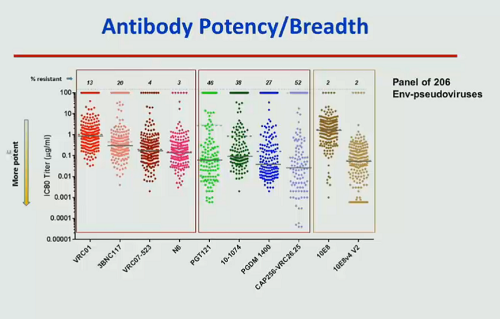
Ciascun bNAb ha una diversa potenza e riesce a neutralizzare percentuali diverse di varianti virali. In alcuni casi, sono pochissimi i ceppi resistenti a un bNAb di spettro particolarmente ampio.
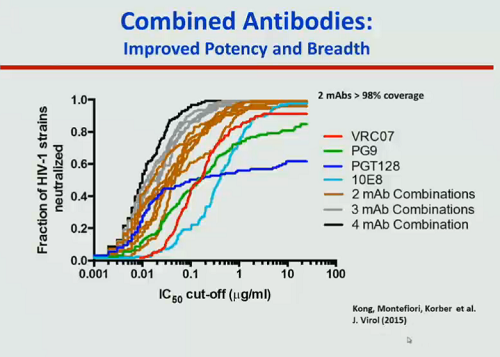
Come superare la resistenza di certi ceppi a certi bNAbs? Ovviamente combinando diversi bNAbs.
Non si è ancora riusciti a trovare una combinazione che arrivi a distruggere il 100% dei ceppi virali, ma vi si è andati molto vicino.
Gli anticorpi possono avere un duplice uso nella clinica: nella prevenzione, per bloccare la trasmissione del virus e così impedire che l’infezione si stabilisca; nel trattamento, per bloccare l’ingresso del virus nelle cellule e per distruggere le cellule infette, sfruttando meccanismi d’azione che potrebbero essere diversi rispetto a quelli utilizzati dagli antiretrovirali (questo è un punto ancora da chiarire).
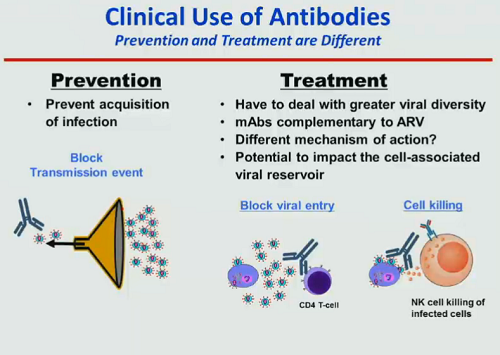
Qualche anno fa si è dimostrato che i bNAbs sono efficaci nei modelli animali, sia nei topi, sia nelle scimmie. Alcune di queste molecole hanno così potuto passare alla fase clinica, mostrando in generale di essere ben tollerati, anche se non sempre efficaci (in qualche partecipante ai trial non hanno avuto nessun effetto e poi si è scoperto che i non-responders ospitavano delle quasispecie virali resistenti a quegli anticorpi).
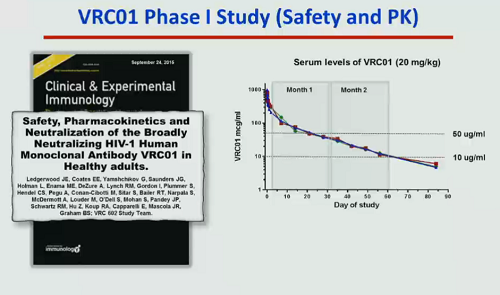
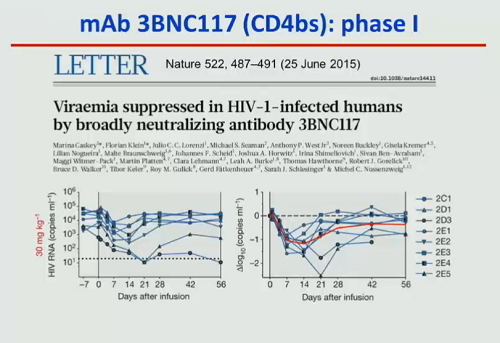
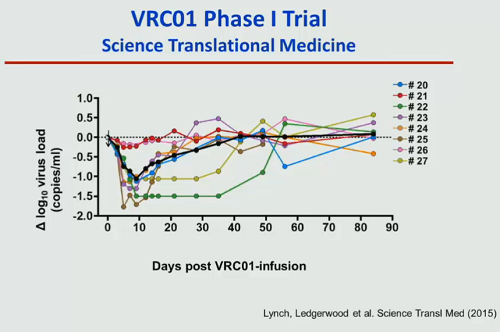
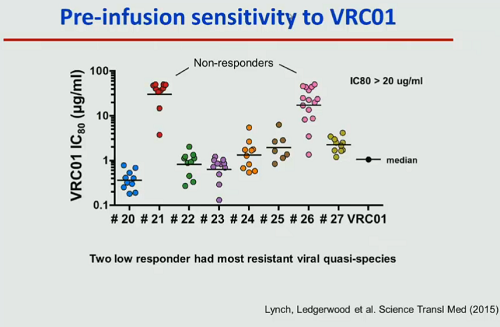
Un tipo di anticorpi un po’ diversi dai vari bNAbs in fase clinica sono degli anticorpi bifunzionali, che hanno la capacità di legarsi sia alle cellule infette, sia a cellule sane in grado di riconoscere e uccidere le cellule infette. Per adesso anche i dati sugli animali sono pochi, ma sono molecole che promettono molto e nei trial sul cancro stanno andando bene ed è presumibile che arrivino presto in fase clinica anche per HIV.
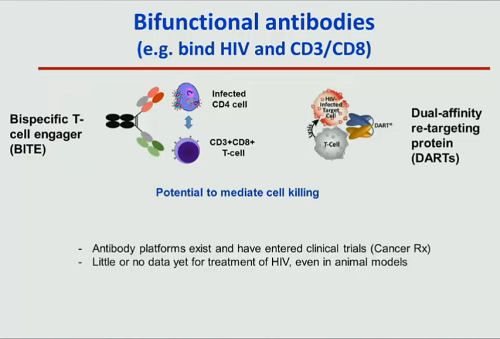

[Vi ricordo che di bNAbs parliamo nel thread Ruolo degli anticorpi monoclonali in una strategia di cura e di anticorpi bifunzionali e proteine DART® (Dual-Affinity Re-Targeting) nel thread Alternative ai vaccini terapeutici per la fase di "kill".]
L’ultima parte della lezione di Koup è dedicata ai CD8 e ai lavori di Louis Picker per creare un vaccino che usi come vettore il CMV.
Koup ricorda il successo ottenuto da Picker con i macachi. Poiché è una ricerca di cui abbiamo parlato a lungo, vi rimando al threa dedicato a Picker e mi limito a postare qui due slides di Koup:
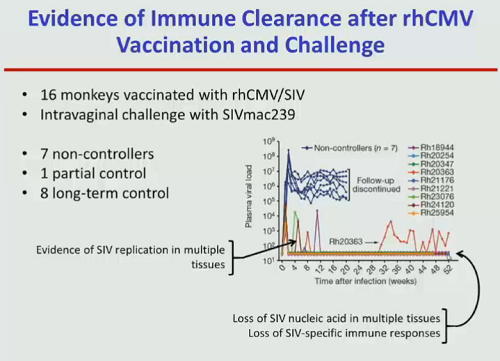

In un nuovo lavoro, pubblicato solo tre settimane fa su Science, Picker ha indagato il meccanismo di protezione che è presumibilmente alla base dell’eradicazione del virus nella metà delle scimmie vaccinate. Anche qui riporto solo le slides di Koup, perché di questo articolo dovremo parlare ancora e ci sarà modo allora di approfondire il discorso (non al CROI perché stranamente, per il secondo anno di seguito, Picker al CROI non presenta nessuna ricerca).


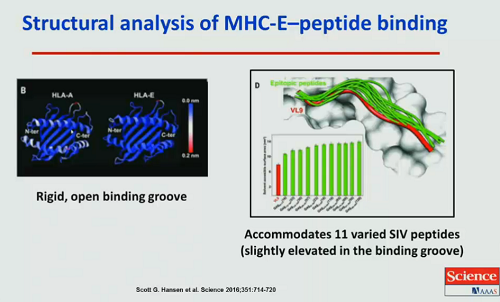
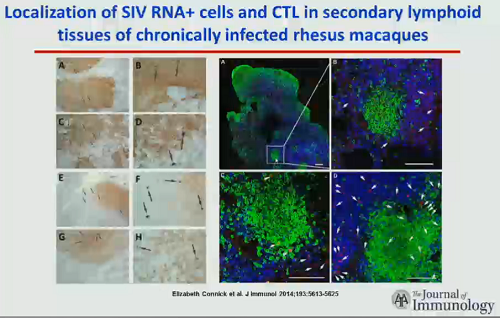
Altra questione correlata ai CD8 che Koup segnala come importante è quella dell’individuazione (sempre da parte del gruppo di lavoro di Picker) di un “santuario” di infezione attiva nei CD4 presenti nei follicoli dei linfociti B, dove i CD8 non riescono ad arrivare. È una ricerca molto bella [e secondo me anche molto meno controversa rispetto al vaccino] di cui abbiamo parlato un anno fa, quindi non mi dilungo, se non per ricordare che anche altri gruppi di lavoro hanno trovato SIV capace di replicazione nei tessuti linfatici dove le reazioni citolitiche dei CD8 non riuscivano ad arrivare: nell’ultima slide si vedono molti CTL SIV-specifici appena fuori dai centri germinali, ma pochissimi all’interno, dove pure si ha replicazione virale.

Koup conclude la sua lezione elencando le domande chiave che attendono una risposta:
Sul microbioma:
- - quali sono le cause della disbiosi nell’infezione da HIV?
- possono essere invertite?
- questo consentirà di avere meno complicanze nel lungo periodo?
Sugli anticorpi neutralizzanti:
- - come si fa a generare bNAbs con un vaccino?
- qual è il meccanismo antivirale degli anticorpi monoclonali ad ampio spettro (bnMAbs)? Inibizione dell’ingresso? Uccisione della cellula?
- l’escape dai bnMAbs pre-esistente prima ancora della loro somministrazione potrebbe affossare il loro uso terapeutico?
Sui CD8:
- - perché metà dei macachi vaccinati con il vaccino rhCMV contro l’SIV non hanno sviluppato alcuna protezione nonostante l’incredibile potenza e ampiezza del vaccino?
- quali strategie possiamo usare per portare più CTL HIV-specifici dentro i centri germinali?