[CROI 2015] J. Coffin: Ricerca di una cura dell’HIV
Inviato: martedì 24 febbraio 2015, 18:52
La lezione che John Coffin, Tuft University, ha tenuto ieri durante il Workshop for New Investigators and Trainees ci introduce alle molte relazioni che ascolteremo sulla ricerca di una cura. Sono argomenti che seguiamo regolarmente, quindi non credo che Coffin ci dirà qualcosa di inaudito, ma la sua è stata una lezione molto chiara, che ha il pregio di sintetizzare i temi di cui abbiamo discusso in un gran numero di thread.
HIV Cure Research

L’esordio di Coffin è il riconoscimento che i farmaci antiretrovirali sono uno dei miracoli della medicina moderna. Nonostante siano un miracolo, però, non fanno miracoli. Infatti, l’unica persona di cui sappiamo con certezza che era infetta da HIV e che ora non lo è più è Timothy Brown, noto come il Berlin Patient.
La sua storia la conosciamo bene, quindi mi limito a ricordarla per sommi punti attraverso questa slide:

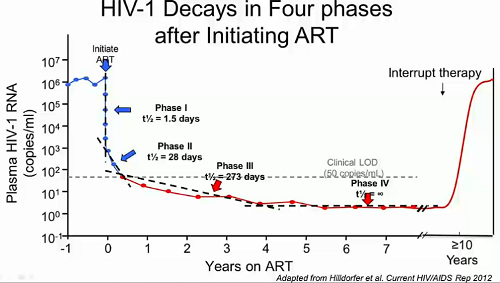
La terapia antiretrovirale, anche se non cura l’infezione, è comunque estremamente efficace nel controllarla: nel giro di poche settimane causa un rapido declino della viremia nel plasma; seguono periodi di più lento declino, durante i quali la viremia si mantiene al di sotto dei livelli di rilevabilità dei test standard. Se però la terapia viene interrotta, il virus ha un rebound piuttosto rapido e torna più o meno agli stessi livelli sui quali si era assestato prima dell’inizio della ART, magari anche dieci anni prima. Questo rebound è quello che impedisce alla terapia di essere una cura.
Coffin passa così a spiegare la natura del reservoir, dandone una definizione molto restrittiva:
Se invece che all’RNA virale guardiamo al DNA (linea gialla nella slide), che cosa accade quando si inizia la ART?
Il suo destino è molto diverso da quello dell’RNA:
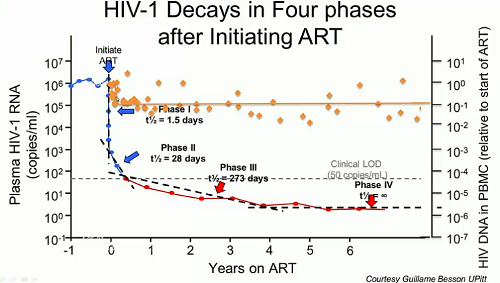
Entrambi declinano rapidamente subito dopo l’inizio della ART, ma mentre l’RNA crolla di più di 10.000 volte, il livello del DNA cala di circa 10 volte rispetto ai valori di prima della terapia.
Questo significa che solo una piccolissima frazione delle cellule che contengono DNA virale (meno di 1 su 100) sono coinvolte nella produzione persistente di virus durante la ART.
Questa minuscola frazione comprende il reservoir che ridà inizio all’infezione quando la terapia viene sospesa.
Coffin passa poi a descrivere il “modello standard” della latenza dell’HIV:
Questa slide mostra la dinamica dell’HIV DNA prima e dopo la ART:
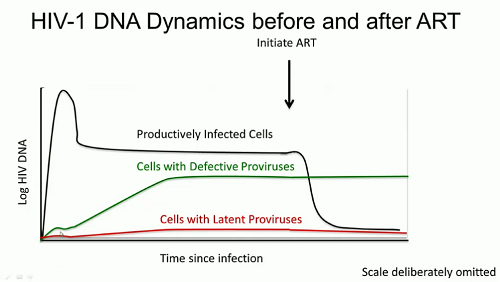
Il problema è che mentre le cellule produttivamente infette muoiono rapidamente, quelle latentemente infette – che contengano o meno provirus in grado di riattivarsi – si accumulano nel tempo.
Si può dunque visualizzare così il DNA virale nelle cellule che vivono più a lungo:
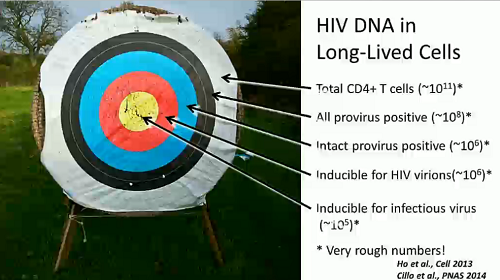
I provirus che possono essere indotti sono pochissimi, ma per arrivare all’eradicazione bisogna riuscire ad eliminarli tutti.
Coffin passa poi a descrivere le proprietà generali dei retrovirus, HIV compreso:
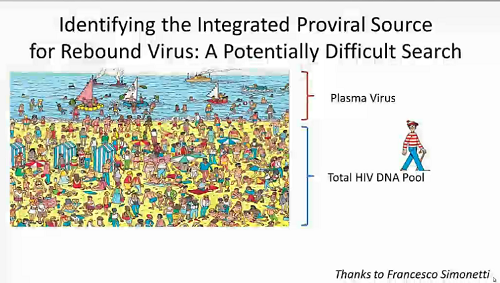
Se solo una piccolissima parte delle cellule DNA positive sono infettate da virus capace di riattivarsi, diventa molto difficile identificare la fonte del rebound del virus quando viene sospesa la ART:

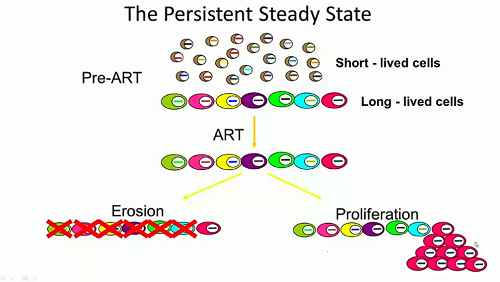
Volendo caratterizzare quello che Coffin chiama “stadio stazionario persistente”, abbiamo che
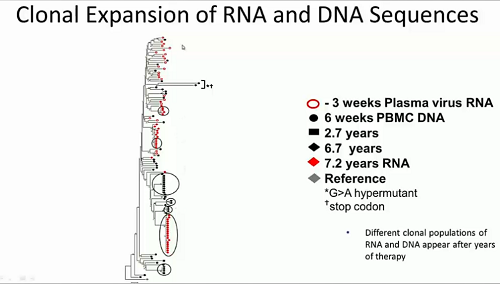
La slide che segue mostra un esempio dell’espansione clonale di sequenze di RNA (in rosso) e di DNA (in nero) dell’HIV in diversi momenti del tempo. Si tratta di espansione clonale della cellula e non di replicazione clonale del virus e si è osservato che popolazioni clonali diverse di HIV RNA e di HIV DNA appaiono anche dopo vari anni di terapia.
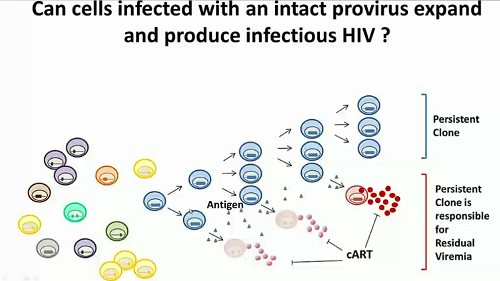
Ancora l’espansione clonale, questa volta illustrata con un disegnino. Questa espansione clonale, stimolata in questo caso antigenicamente, può dare vita a cellule che contengono virus infettivo, capace di riattivarsi:
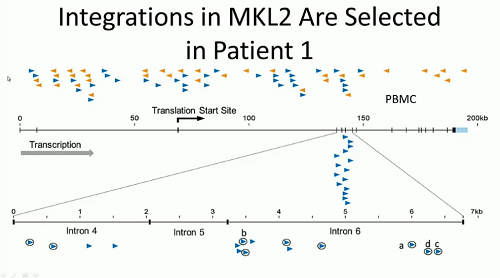
Una questione che verrà ampiamente discussa durante il congresso è quella del sito di integrazione del virus. In alcuni pazienti, se si guardano le cellule mononucleate del sangue periferico infette e messe a coltura, si osserva una particolare distribuzione dei siti di integrazione: mentre in genere si distribuiscono attraverso tanti geni diversi, in questi casi si concentrano in una piccolissima regione del genoma, che si ritiene venga selezionata dall’espansione clonale:
Come colpire i provirus latenti? L’immagine scelta da Coffin per illustrare la situazione in cui si trova la ricerca non ha bisogno di grandi commenti: l’arciere cieco

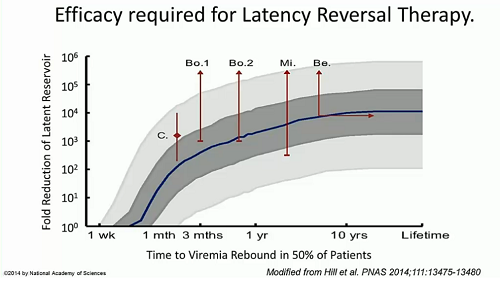
Coffin parla di un lavoro del gruppo di Siliciano uscito l’anno scorso per valutare l’efficacia nel ridurre le dimensioni del reservoir che si richiede a una terapia di inversione della latenza se si vuole rimandare di un mese, 3 mesi … 10 anni o tutta la vita il rebound della viremia dopo la sospensione della ART. Se si riduce il reservoir di 10.000 volte, ci si può attendere il rebound della viremia in un anno. Se si vuole arrivare a una cura accettabile, la riduzione del reservoir deve probabilmente essere nell’ordine delle 100.000 volte (Bo.1 e Bo.2 sono i Boston Patients, Mi. la Mississippi Baby, Be. il Berlin Patient).
Le strategie di cura che Coffin elenca le conosciamo bene:
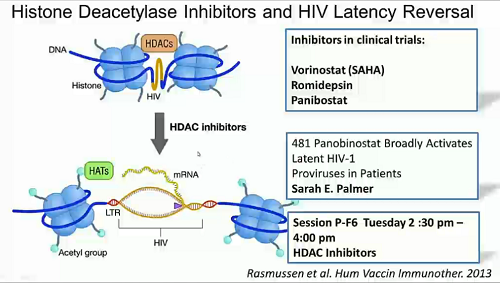
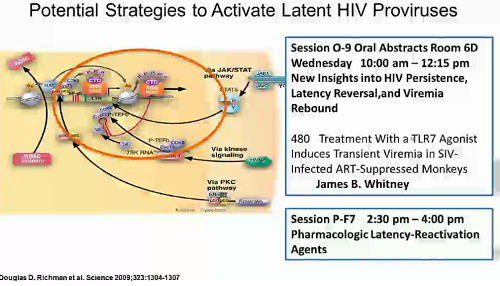
E conosciamo bene gli strumenti finora adottati per perseguire quelle strategie: farmaci antilatenza che sfruttano diversi meccanismi d’azione, terapia genica con modificazione delle cellule staminali, vaccinazioni che stimolino le risposte CTL … tutte cose che vedremo nei dettagli durante il congresso. Bastino, allora, le slides:

Le grandi domande ancora in attesa di una risposta:
HIV Cure Research

L’esordio di Coffin è il riconoscimento che i farmaci antiretrovirali sono uno dei miracoli della medicina moderna. Nonostante siano un miracolo, però, non fanno miracoli. Infatti, l’unica persona di cui sappiamo con certezza che era infetta da HIV e che ora non lo è più è Timothy Brown, noto come il Berlin Patient.
La sua storia la conosciamo bene, quindi mi limito a ricordarla per sommi punti attraverso questa slide:

La terapia antiretrovirale, anche se non cura l’infezione, è comunque estremamente efficace nel controllarla: nel giro di poche settimane causa un rapido declino della viremia nel plasma; seguono periodi di più lento declino, durante i quali la viremia si mantiene al di sotto dei livelli di rilevabilità dei test standard. Se però la terapia viene interrotta, il virus ha un rebound piuttosto rapido e torna più o meno agli stessi livelli sui quali si era assestato prima dell’inizio della ART, magari anche dieci anni prima. Questo rebound è quello che impedisce alla terapia di essere una cura.

Coffin passa così a spiegare la natura del reservoir, dandone una definizione molto restrittiva:
- - il termine “reservoir” dovrebbe essere usato solo alle cellule e al virus che si ripresenta quando la ART viene sospesa;
- la persistenza in sé non può essere attribuita alla replicazione attiva del virus. Il reservoir deve dunque consistere di cellule che sono longeve e che contengono dei provirus dell’HIV non difettivi, in uno stato che non è espresso, ma che è inducibile (“latente”);
- queste cellule non sono create dalla ART, né sono indotte ad esprimere il virus dalla cessazione della ART;
- sono solo una piccola parte del totale delle cellule che contengono DNA virale (forse l’1%, o anche meno), la grande maggioranza delle quali contengono provirus difettivi, alcuni dei quali possono essere espressi come RNA;
- NON si può ritenere che la maggioranza delle cellule DNA positive riflettano le caratteristiche di quelle cellule infette che costituiscono il reservoir (bisogna quindi stare molto attenti quando si interpretano i risultati di esperimenti che valutano il DNA virale presente nelle cellule);
- circa 1 su 1 milione di CD4 quiescenti contengono dei provirus che possono essere indotti da esperimenti ex vivo. Che dire di altri tipi di cellule? Forse i macrofagi?
Se invece che all’RNA virale guardiamo al DNA (linea gialla nella slide), che cosa accade quando si inizia la ART?
Il suo destino è molto diverso da quello dell’RNA:

Entrambi declinano rapidamente subito dopo l’inizio della ART, ma mentre l’RNA crolla di più di 10.000 volte, il livello del DNA cala di circa 10 volte rispetto ai valori di prima della terapia.
Questo significa che solo una piccolissima frazione delle cellule che contengono DNA virale (meno di 1 su 100) sono coinvolte nella produzione persistente di virus durante la ART.
Questa minuscola frazione comprende il reservoir che ridà inizio all’infezione quando la terapia viene sospesa.
Coffin passa poi a descrivere il “modello standard” della latenza dell’HIV:
- - la grande maggioranza delle cellule infette muore nel giro di pochi giorni;
- una piccola minoranza di cellule infette entra in uno stato di quiescenza che – per molte possibili ragioni, non tutte note - sopprime l’espressione del provirus;
- una grande minoranza di cellule sono infette con provirus che presentano delle mutazioni che li disattivano;
- queste cellule sono molto longeve e possono essere stimolate ad espandersi mediante segnali antigenici o omeostatici;
- i provirus latenti intatti rilasciano piccole quantità di virus, sia in modo continuo, sia più verosimilmente con delle esplosioni che fanno seguito a qualche tipo di stimolo;
- queste possono essere rilevate ex vivo se si attivano i CD4 quiescenti estratti da persone che sono in terapia da lungo tempo.
Questa slide mostra la dinamica dell’HIV DNA prima e dopo la ART:

Il problema è che mentre le cellule produttivamente infette muoiono rapidamente, quelle latentemente infette – che contengano o meno provirus in grado di riattivarsi – si accumulano nel tempo.
Si può dunque visualizzare così il DNA virale nelle cellule che vivono più a lungo:

I provirus che possono essere indotti sono pochissimi, ma per arrivare all’eradicazione bisogna riuscire ad eliminarli tutti.
Coffin passa poi a descrivere le proprietà generali dei retrovirus, HIV compreso:
- - si replicano attraverso DNA intermedio stabilmente integrato;
- il ciclo di replicazione è in qualche modo soggetto ad errori, che comportano mutazioni, così HIV accumula diversità durante ripetuti cicli di replicazione;
- il provirus integrato si replica insieme al DNA della cellula ed è geneticamente molto stabile;
- pertanto, uno specifico provirus può “etichettare” i cloni di cellule infette e può sopravvivere quanto sopravvive la cellula infetta;
- l’espressione dei provirus per creare virus può essere regolata dalla struttura della cromatina e da altre caratteristiche epigenetiche;
- la ART blocca l’infezione e la formazione del provirus, ma non ha alcun effetto sulle cellule che sono già state infettate;
- questo consente lunghi periodi di sopravvivenza dell’infezione nelle cellule latentemente infette più longeve;
- una questione aperta è se i provirus dell’HIV stessi influenzino la sopravvivenza e la crescita delle cellule in base ai siti di integrazione.
Se solo una piccolissima parte delle cellule DNA positive sono infettate da virus capace di riattivarsi, diventa molto difficile identificare la fonte del rebound del virus quando viene sospesa la ART:


Volendo caratterizzare quello che Coffin chiama “stadio stazionario persistente”, abbiamo che
- - nel periodo che precede la ART abbiamo un gran numero di cellule poco longeve, in cui il provirus muore in fretta, e una relativamente più piccola frazione di cellule che hanno una vita più lunga, in cui il provirus ha una durata corrispondente;
- l’inizio della ART non influisce sulle cellule infette, ma ha l’effetto di rende più “visibili” quelle che contengono provirus;
- si ha poi da un lato una graduale per quanto lenta erosione di quelle cellule, dall’altro una proliferazione clonale delle cellule infette sopravvissute, sia grazie a stimolazione antigenica, sia grazie a proliferazione omeostatica;
- il numero di cellule infette rimane così pressappoco lo stesso; si ha però l’emergere di una popolazione di cloni.

La slide che segue mostra un esempio dell’espansione clonale di sequenze di RNA (in rosso) e di DNA (in nero) dell’HIV in diversi momenti del tempo. Si tratta di espansione clonale della cellula e non di replicazione clonale del virus e si è osservato che popolazioni clonali diverse di HIV RNA e di HIV DNA appaiono anche dopo vari anni di terapia.

Ancora l’espansione clonale, questa volta illustrata con un disegnino. Questa espansione clonale, stimolata in questo caso antigenicamente, può dare vita a cellule che contengono virus infettivo, capace di riattivarsi:

Una questione che verrà ampiamente discussa durante il congresso è quella del sito di integrazione del virus. In alcuni pazienti, se si guardano le cellule mononucleate del sangue periferico infette e messe a coltura, si osserva una particolare distribuzione dei siti di integrazione: mentre in genere si distribuiscono attraverso tanti geni diversi, in questi casi si concentrano in una piccolissima regione del genoma, che si ritiene venga selezionata dall’espansione clonale:

Come colpire i provirus latenti? L’immagine scelta da Coffin per illustrare la situazione in cui si trova la ricerca non ha bisogno di grandi commenti: l’arciere cieco

Coffin parla di un lavoro del gruppo di Siliciano uscito l’anno scorso per valutare l’efficacia nel ridurre le dimensioni del reservoir che si richiede a una terapia di inversione della latenza se si vuole rimandare di un mese, 3 mesi … 10 anni o tutta la vita il rebound della viremia dopo la sospensione della ART. Se si riduce il reservoir di 10.000 volte, ci si può attendere il rebound della viremia in un anno. Se si vuole arrivare a una cura accettabile, la riduzione del reservoir deve probabilmente essere nell’ordine delle 100.000 volte (Bo.1 e Bo.2 sono i Boston Patients, Mi. la Mississippi Baby, Be. il Berlin Patient).

Le strategie di cura che Coffin elenca le conosciamo bene:
- - “Shock and kill” – con l’attivazione del provirus latente continuando la ART, la necessità che o l’espressione virale o la risposta immune uccidano le cellule infette, l’eventuale sospensione della ART;
- sospensione della ART dopo “immunizzazione” per evitare che il virus ricominci a replicarsi – e quindi terapia genica che renda non infettabili le cellule target, “vaccinazione terapeutica”, somministrazione di anticorpi monoclonali.
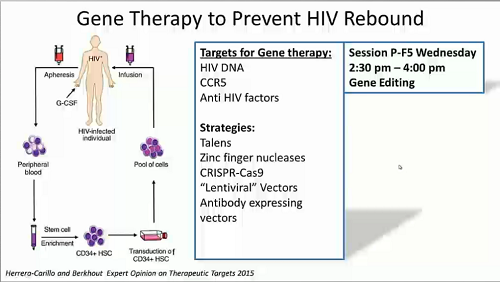
E conosciamo bene gli strumenti finora adottati per perseguire quelle strategie: farmaci antilatenza che sfruttano diversi meccanismi d’azione, terapia genica con modificazione delle cellule staminali, vaccinazioni che stimolino le risposte CTL … tutte cose che vedremo nei dettagli durante il congresso. Bastino, allora, le slides:




Le grandi domande ancora in attesa di una risposta:
- 1. In quali cellule si nasconde il reservoir latente? Dov’è? Quanto è grande?
2. Le cellule latentemente infette sono capaci di espansione clonale?
3. Una qualsiasi ipotizzabile strategia shock and kill è abbastanza potente da eliminare tutte le cellule latentemente infette (~10^5)?
4. Se la risposta è no, allora qual è la migliore strategia per bloccare la ricomparsa del virus se la ART viene interrotta?