È tema di grande interesse sia negli studi sulla cura, in cui un'interruzione terapeutica è al momento richiesta per poter valutare gli effetti dei trattamenti sperimentati, sia nei casi in cui persone entrate in terapia durante la fase acuta dell'infezione desiderino provare a interrompere la ART. A volte, infatti, si ha un rebound quasi immediato della viremia, proprio come accade in genere alle persone che hanno iniziato la ART durante la fase cronica, A volte, invece, il rebound della viremia è molto dilazionato, o addirittura non c'è. Capire prima chi si candida a diventare un "post treatment controller" può essere di grande ultilità per valutare l'opportunità o meno della sospensione degli antiretrovirali.
Trovare e validare uno o più marker che indichino i probabili tempi del rebound è dunque l'obiettivo di ricerche come quelle presentate in questo thread.
Del lavoro dello SPARTAC abbiamo già iniziato a parlare l'autunno scorso, quindi riporto qui alcune cose scritte nel thread The RIVER Trial (CHERUB). Seguiranno i post dedicati alla presentazione al CROI di John Frater e a quella di Jonathan Li.
In sintesi:Dora ha scritto:A settembre, John Frater e colleghi hanno pubblicato su eLife HIV-1 DNA predicts disease progression and post-treatment virological control.
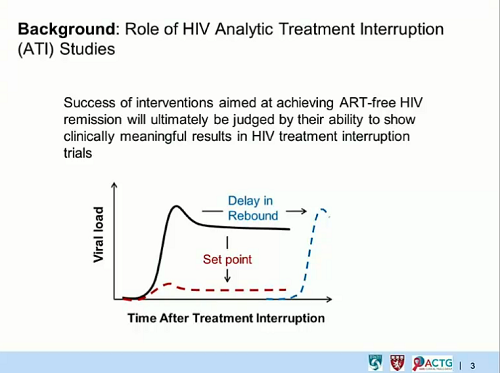
Mi era sfuggito, ma la pubblicazione - sempre su eLife – la settimana scorsa di un commento di Steven Deeks e Leslie Cockerham (Biomarker reveals HIV's hidden reservoir) me lo ha ricordato. E dal commento di Deeks ho riadattato la figura che segue, in cui si introduce il lavoro di Frater:
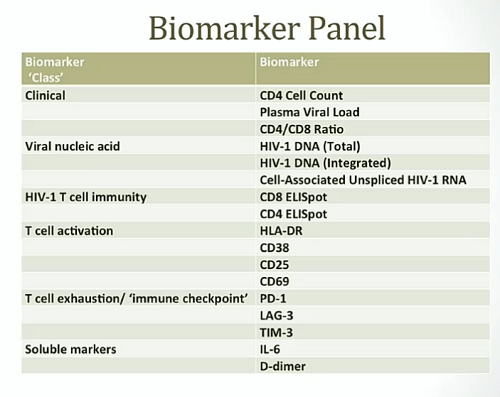
Per eradicare le cellule latentemente infette, dunque, dobbiamo anzitutto essere capaci di sapere quante ce ne sono. La maggior parte delle persone in terapia da lungo tempo hanno fra le 10 e le 1000 copie di HIV DNA per milione di CD4. Ma la gran parte di questo DNA virale è difettivo, quindi non potrà mai dare inizio a nuovi cicli di infezione. Quello che davvero serve è pertanto capire quante sono quelle rare cellule che contengono HIV DNA intatto e che può essere indotto a produrre nuovi virus.
Per arrivare a questo serve un marker biologico, cioè una specifica molecola, che distingua le cellule del reservoir latente dalle altre cellule infette.
In assenza di questo marker, l’unico modo per sapere se un intervento terapeutico ha effettivamente curato un paziente, riducendo o addirittura eliminando il reservoir, è l’interruzione della ART e l’attesa del rebound virale, con i rischi che questo comporta sia per il paziente, sia per i suoi partner.
Esistono diversi metodi per misurare il reservoir di HIV, che vanno dalla semplice stima di DNA virale associato alle cellule mediante PCR quantitativa (qPCR) fino ai molto più complessi Viral Outgrowth Assay (VOA) di Siliciano, che sono considerati il gold standard, ma sono costosissimi e richiedono tempi molto lunghi, passando per la misura dell’HIV RNA intracellulare, che riflette in modo più accurato l’effettiva capacità di una cellula infetta di produrre nuovi virioni.
Indipendentemente dal tipo di test usato, mentre la misurazione della viremia plasmatica e del numero dei CD4 sono buoni marker surrogati della progressione clinica dell’infezione, l’utilità clinica di misurare il reservoir non è ben chiara. Dal momento, però, che il DNA virale associato alle cellule precede la viremia plasmatica durante il ciclo vitale del virus, è logico chiedersi se la misura dell’HIV DNA (come surrogato delle dimensioni del reservoir) possa avere una rilevanza clinica. Inoltre, avere un marker surrogato del reservoir può servire nelle sperimentazioni cliniche per arrivare a una cura per valutare l’efficacia degli interventi terapeutici.
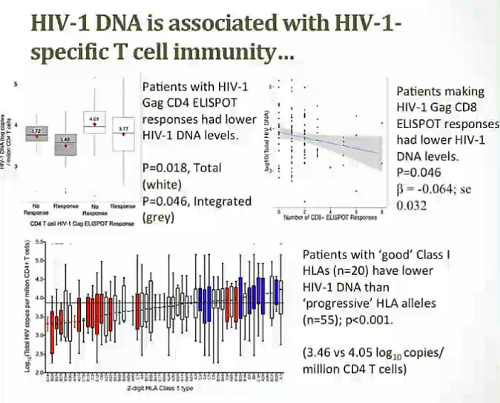
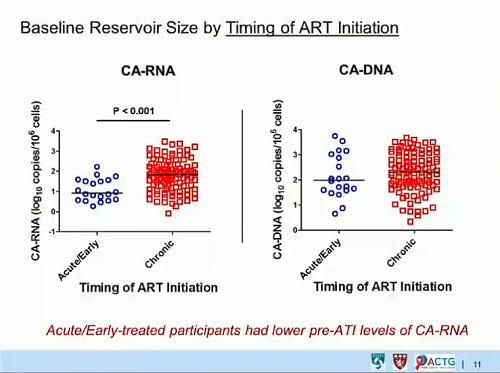
Quello che Frater e colleghi dello studio SPARTAC hanno dunque fatto è stato di misurare la frequenza di CD4 del sangue periferico contenenti HIV DNA (cioè l’HIV DNA totale) in tutti i partecipanti all’inizio dello studio, ipotizzando che, anche se la maggior parte di questo DNA virale è difettivo e dunque incapace di replicazione, il DNA totale nell’infezione da HIV iniziale e non ancora trattata con antiretrovirali possa predire il modo in cui la malattia progredirà.
- E in effetti, come ci si aspettava, il DNA totale è diminuito di molte volte durante il trattamento con la ART. Inoltre, il DNA totale misurato subito prima di interrompere la ART ha predetto sia quanto rapidamente il numero dei CD4 sarebbe diminuito, sia quanto rapidamente si sarebbe verificato il rebound della viremia.
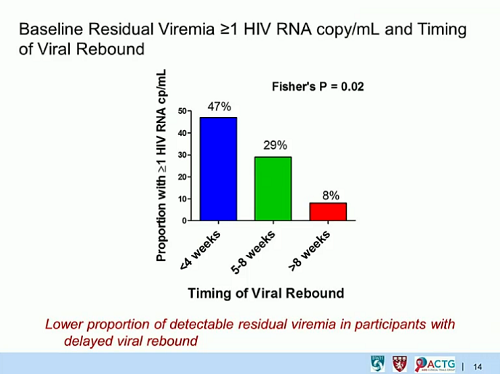
Chi aveva alti livelli di DNA totale ha avuto un tasso più che doppio di rebound virale rispetto a chi aveva bassi livelli di DNA totale.
Il livello di HIV DNA totale può dunque predire quanto a lungo un paziente può rimanere in sospensione terapeutica senza avere problemi e può essere usato per identificare i pazienti che sono a maggiore rischio di rapido rebound ed è improbabile che possano avere benefici da un’interruzione della ART.
Ci sono in programma degli studi per confermare quanto osservato da Frater e colleghi. Se questo marker verrà validato, l’HIV DNA totale potrà essere usato per monitorare i prossimi tentativi di arrivare a una cura.
Dora ha scritto:avere dimostrato (o confermato) in uno studio con un numero consistente di pazienti
direi che dà un gran numero di informazioni utili per capire il ruolo dell'HIV DNA.
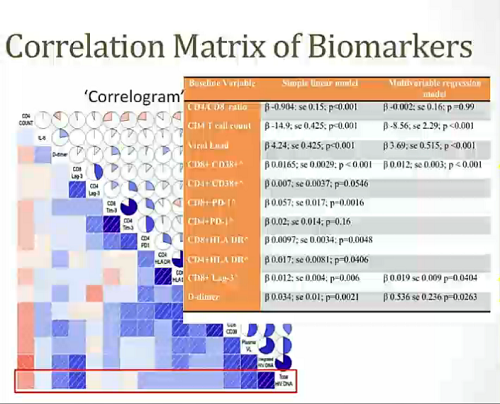
- - che i livelli di HIV DNA prima della ART si associano a VL e a CD4, i tipici marker di progressione,
- che l'HIV DNA predice la progressione nei pazienti non trattati,
- che l'HIV DNA declina durante la ART,
- che l'HIV DNA valutato nel momento in cui si interrompe la ART predice la progressione clinica,
- che l'HIV DNA aumenta da quando si interrompe la ART,
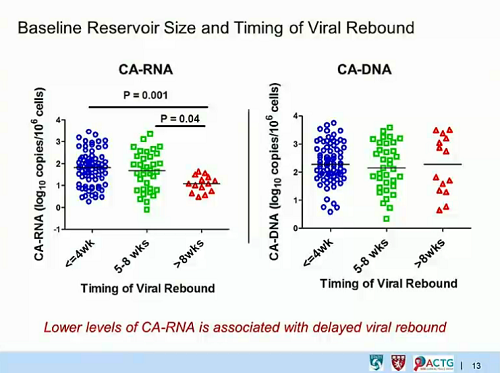
- che l'HIV DNA misurato nel momento in cui si interrompe la ART predice il momento del rebound della viremia nel plasma ...
- ... e che tutto questo accade indipendentemente dalla presenza di quantità non definite di DNA virale difettivo,