******************
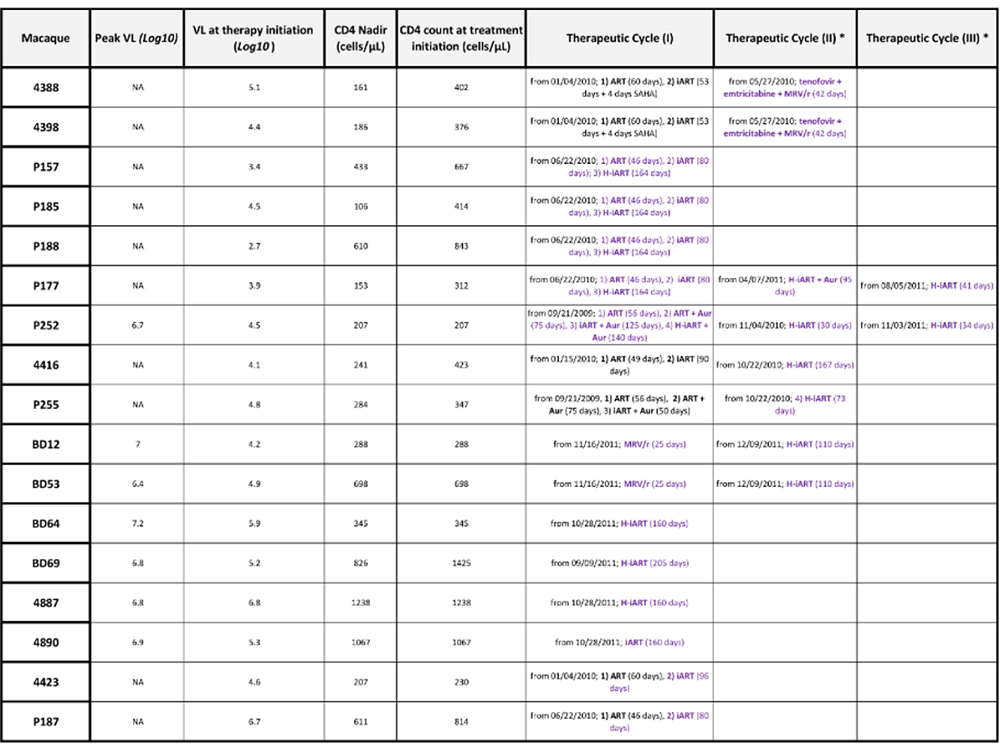
La ricerca che Andrea Savarino e il suo collaboratore Iart Shytaj hanno portato al workshop sui reservoir di Miami - Pharmacologically Induced Functional Cure-like Condition in Chronically SIVmac251 Infected Macaques is Associated with Immune Reconstitution and Broad Anti-Gag Immune Responses Increasing over Time - è un approfondimento di quanto già pubblicato l’estate scorsa sul controllo che alcuni macachi con infezione cronica da SIV sono riusciti a mantenere sulle viremie dopo essere stati trattati con H-iART (tenofovir, emtricitabina, raltegravir, darunavir/r e maraviroc) + auranofin + BSO (butionina sulfossimina).
Ho approfittato della gentilezza del dottor Savarino per chiedergli di mandarmi le slides e insieme rispondere a un paio di domande sulle prospettive future della sua ricerca.
Prima quello che io sono riuscita a trarre dalle diapositive, poi le domande.
Poiché il controllo delle viremie osservato si è associato a un aumento delle risposte immuni anti-Gag e si è verificato in presenza dei CD8, l’approfondimento è consistito nell’analisi dell’evoluzione a lungo termine dei parametri viro-immunologici sia dei macachi che hanno risposto alla terapia “completa”, sia di quelli che sono stati trattati solo con H-iART, o con l’aggiunta del solo auranofin.
Prima di essere sottoposte al trattamento, tutte le scimmie mostravano delle risposte immuni anti-Gag o basse o addirittura non rilevabili, mentre fino a un anno dopo la fine di un singolo ciclo della terapia versione deluxe i livelli delle risposte anti-Gag hanno continuato a crescere nel tempo. L’immunità cellulare diretta contro la Gag sembra proprio che dia un contributo fondamentale al controllo della viremia.
Nulla di simile si è visto nei macachi che non hanno ricevuto la BSO, o cui questa è stata somministrata separatamente dall’auranofin.
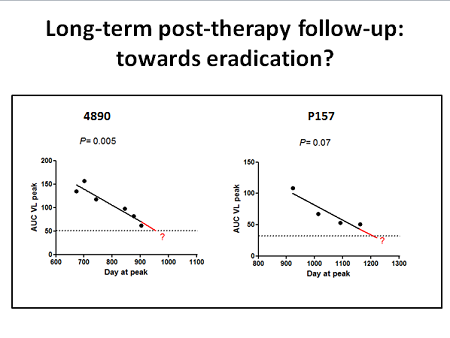
Il macaco che partiva dal set point virale più alto prima della terapia è rimasto in osservazione per un periodo di follow up più lungo (un anno) e ha presentato un nuovo set point (a 5 mesi) molto più basso rispetto a quello di partenza (1,4 log di SIV RNA/mL di sangue, con una diminuzione di ben 4,7 log rispetto ai livelli di prima della terapia) – e questo coerentemente con la continua diminuzione del set point virale e il continuo aumento dei CD4, nonché con l’aumento delle risposte anti-Gag specifiche.
Rimangono però delle questioni aperte, che riguardano sostanzialmente
- 1. Una migliore definizione dei meccanismi di azione di questa terapia, perché quel che si è visto finora è che la ART+auronofin fa diminuire le dimensioni del reservoir dei CD4; che l’auranofin induce in parte una distruzione selettiva dei CD4 memoria (sia Tcm, sia Tem) e che la ART+auranofin+BSO migliora le risposte immuni cellulo-mediate anti-Gag (e questo va parallelamente alla riduzione delle viremie); e infine che non si sono osservate correlazioni fra il controllo delle viremie e i titoli degli anticorpi neutralizzanti.
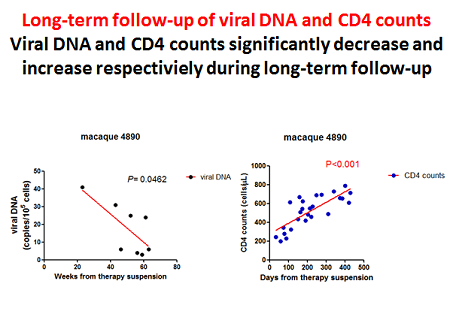
2. Una possibile questione critica che già era stata messa in luce nell’articolo dell’estate scorsa su Retrovirology è quella che riguarda il numero dei CD4 dopo il trattamento, perché è vero che fra le slides dedicate ai meccanismi di azione ce n’è una che ci mostra come nel macaco 4890 il DNA virale e il numero dei CD4 siano rispettivamente diminuiti e aumentati durante il periodo di follow up,
ma è anche vero che in uno su tre dei macachi “funzionalmente curati” i CD4 sono rimasti molto bassi e che nell’articolo Savarino temeva che questo possa essere, sul modello di alcuni elite controller, un prezzo – ancorché non troppo caro - da pagare per poter mantenere la viremia sotto controllo.
3. Bisogna ancora valutare il follow up a lungo termine del DNA virale – e qui si gioca la possibilità di controllare davvero il virus e magari anche eradicarlo. La domanda conclusiva che Savarino si pone è infatti SE IN UNA SITUAZIONE IN CUI IL RESERVOIR DIMINUISCE E L’IMMUNITÀ MIGLIORA SIA POSSIBILE CHE IL SISTEMA IMMUNITARIO RIESCA A CONTROLLARE DA SOLO L’INFEZIONE, MAGARI FINO AL PUNTO DI ERADICARLA.
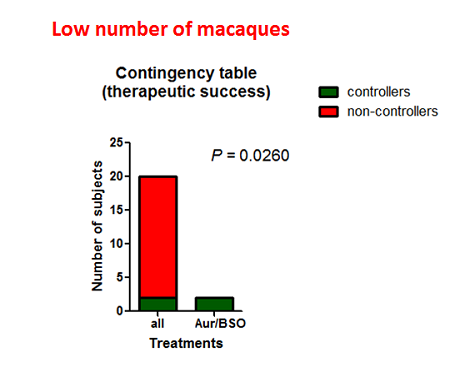
4. Il numero sia delle scimmie totali, sia di quelle che hanno tratto giovamento dalla terapia completa, è ancora piuttosto basso.
La conclusione di Savarino è che i risultati ottenuti con la somministrazione della terapia “completa” possono essere interpretati come lo stabilirsi di una condizione che può essere definita di “cura funzionale”, con un progressivo miglioramento del controllo della viremia durante il periodo di follow up dopo il trattamento e con un periodo di remissione della malattia dopo la fine del trattamento che si sta dimostrando piuttosto lungo.
In una delle slides si parla del “potenziale curativo” di questo tipo di trattamento e si elencano tre punti principali:
- 1. Alta scalabilità: il trattamento dura tre mesi e tutti i farmaci possono essere assunti per bocca (tranne la BSO, che deve essere infusa);
2. Buon profilo di sicurezza: l’auranofin è in uso da anni per trattare l’artrite reumatoide e la BSO è stata ben tollerata in trial clinici di fase I; la combinazione dei due farmaci è stata ben tollerata nei topi e, insieme alla ART, sono stati ben tollerati nelle scimmie;
3. Limitata ospedalizzazione necessaria: non servono né operatori sanitari altamente qualificati, né infrastrutture particolarmente costose.
******************
Come dicevo prima, ho approfittato della disponibilità del dottor Savarino per rivolgergli alcune domande sul futuro di questa ricerca. Ed ecco le sue risposte.
● Quando lo scorso luglio è uscito l’articolo su Retrovirology, nel comunicato stampa che lo accompagnava si diceva che stavate programmando l’inizio della sperimentazione clinica per i primi mesi del 2014. Poi nei mesi scorsi la lettera al Ministro della Salute scritta dal presidente dell’associazione “Sportello dei Diritti”, Giovanni D'Agata, e il breve scambio che ne è seguito hanno fatto pensare che ci sia ancora qualcosa che sta bloccando l’inizio della fase clinica. È così? Si tratta di ragioni scientifiche, di mancanza di finanziamenti o di che altro?
Purtroppo, mi duole assai far notare che in Italia ben poco si spiega con motivazioni eminentemente scientifiche. Se le ragioni del mancato interessamento ad ora mostrato dal Ministero della Salute fossero solo scientifiche, allora mi chiederei perché il Ministero non ascolti proprio il mio gruppo, che, per indici bibliografici come l’impact factor (un punteggio assegnato al tipo di pubblicazioni) è tra i primi in Italia nel settore HIV/AIDS, e forse il primo se si standardizza l’impact factor al numero di unità di personale dedicate alla ricerca. Per fare un esempio, i risultati delle sperimentazioni cliniche sui “vaccini” Tat e pediatrico sono stati pubblicati sulla rivista PLOS One, che ha un impact factor di 3.7, di molto inferiore alle riviste specialistiche di massimo impatto nel settore HIV/AIDS, che sono AIDS, Retrovirology e PLOS Pathogens.
Vi è un mancato supporto generale, che non riguarda solo il Ministero. Per esempio, Iart Shytaj, il primo autore di tre fra i nostri più importanti articoli scientifici, non è stato ritenuto meritevole di ricevere una borsa di studio in un concorso pubblico bandito da ANLAIDS. Fra l’altro Iart è stato, per la seconda volta, selezionato da una commissione internazionale per parlare al convegno HIV Persistence during Therapy (quest’anno tenutosi a Miami), tra i massimi esperti mondiali, presentando una relazione di cui discuteremo qui.
Nonostante i travisamenti di una certa stampa minore e di alcuni titolisti, non ho mai promesso una cura per l’AIDS, ma ritenevo che i risultati sulle scimmie meritassero un’attenzione maggiore da parte di varie istituzioni italiane. Forse per essere considerati bisogna spararla grossa e promettere miracoli come hanno fatto altri, ma io non lo farò mai. Per ora, anche alla luce dei risultati finali dei “pazienti di Boston” e del fallimento del clinical trial sul vorinostat, annunciati, rispettivamente da Timothy Heinrich e da David Margolis al convegno di Miami, la cura per l’AIDS umana in fase cronica non esiste ancora, anche se, forse per la prima volta, vi sono strategie promettenti su cui iniziare a scommettere.
● Mi interessa molto sapere qualcosa su come verrà impostato il trial clinico:
- • Quanti pazienti pensate di arruolare?
• Quali saranno le condizioni di inclusione e di esclusione?
• Il rischio segnalato nell’articolo su Retrovirology che i CD4 non aumentino molto a seguito del trattamento con H-iART/auranofin/BSO può costituire una ragione di esclusione di alcuni pazienti?
• Quali saranno gli end point della sperimentazione?
• Quali i tempi previsti?
- a) Il nostro protocollo originale prevedeva di arruolare tra i 10 e i 20 pazienti in uno studio “open label”.
b) I pazienti devono essere sotto terapia antiretrovirale con carica virale stabilmente soppressa (la soglia dovrebbe essere quella standard di 50 copie/ml). Il tipo di ART a cui il paziente è sottoposto non costituirà probabilmente motivo di esclusione. In questa prima fase verranno esclusi pazienti con mutazioni di farmacoresistenza ai principali farmaci antiretrovirali, quelli con patologie renali e quelli con lupus eritematoso (che potrebbero avere reazioni collaterali all’uso di auranofin).
c) Qualora questa prima fase del clinical trial preveda la sospensione di terapia, verrà somministrato un breve ciclo di ART al rebound del virus (seguendo il rationale di Shytaj et al. PLOS Pathogens 2012), in modo da cercare di prevenire sia la ricostituzione del reservoir virale sia un eventuale calo dei CD4. In ogni caso i dati presentati a Miami dal Dr. Shytaj dimostrano che il calo dei CD4 è temporaneo e che, in concomitanza con il calo della viral load e del DNA virale, i CD4 risalgono a livelli normali (seppur lentamente). Pertanto la soglia di esclusione basata sui livelli di CD4 non sarà particolarmente stringente (probabilmente intorno ai 500/microlitro di sangue).
d) Gli end point sono in primo luogo la verifica della sicurezza e tollerabilità della terapia. In secondo luogo gli effetti della terapia sui livelli di DNA provirale a tre mesi dall’inizio della terapia e, in terza istanza (ma solo in presenza delle risorse necessarie), l’eventuale verifica di un effetto sui livelli del set point virale in seguito a sospensione della terapia dopo l’aggiunta di BSO.
La sperimentazione clinica inizierà, in due paesi esteri, come studio “proof of concept” sulla tollerabilità di auranofin + ART e sul suo potenziale impatto sul reservoir. Riallacciandomi a quanto ho detto prima, dato che, almeno per ora, l’intero carico economico della sperimentazione graverà su fondi esteri, sarà saggiato solo auranofin. Sarebbe stato bello aggiungere anche BSO e sospendere le terapie, ma ciò prevedrebbe un’ospedalizzazione che, per quanto breve, alzerebbe i costi. Io parteciperò scientificamente, ma, non avendo voce in capitolo sul lato economico, dovrò adeguarmi alle decisioni di altri. Non mi è pertanto possibile, al momento, fare previsioni sulle tempistiche della sperimentazione di auranofin e BSO. Per quanto riguarda lo studio proof of concept di auranofin, prevedo (ma non posso giurare) che si possa iniziare nella prima metà del 2014 in almeno uno dei due paesi coinvolti (Brasile e USA). Comunque io non sarò il direttore di questi studi e pertanto non avrò potere di arruolamento. Ho ricevuto, nel corso di questi mesi centinaia di messaggi da parte di persone che vivono con HIV/AIDS e che vogliono apportare un miglioramento alle loro vite. Cogliendo l’occasione di questa intervista, voglio dire ai pazienti italiani che mi dispiace infinitamente non poter dare loro le desiderate informazioni circa l’inizio di una sperimentazione clinica in Italia. Io ce l’ho messa davvero tutta, ma la cosa trascende ogni mio controllo.
● State valutando il follow up a lungo termine del DNA virale? Su che cosa lavorerete adesso? Per esempio, ritenete di dover approfondire la questione, di cui avete discusso a Miami, del ruolo dell’immunità cellulare diretta contro la Gag dell’SIV? Se, come avete dimostrato, le risposte anti-Gag stimolate dal trattamento con H-iART/auranofin/BSO sono ciò che ha permesso il buon controllo della viremia in alcuni macachi, c’è modo di aumentare queste risposte? E di stimolarle nei macachi che non hanno risposto bene al trattamento?
Di questo ramo della ricerca si sta occupando il mio collaboratore, il succitato Iart Shytaj. Il progetto (ovvero quello non finanziato da ANLAIDS) prevedeva anche il follow-up del DNA virale. Se ci riusciremo, lavoreremo comunque su un’ulteriore caratterizzazione della risposta immunitaria dei macachi trattati con auranofin e BSO (confrontandola con quella di alcuni controlli) e in generale sull’analisi dello stato immunitario che accompagna il controllo della viremia a seguito di sospensione di terapia (marker di attivazione, proliferazione etc.). Inoltre stiamo attendendo da un laboratorio americano i risultati del sequenziamento del virus che emerge nei vari “blip” (che sono poi controllati dal sistema immunitario), per capire se si tratti di episodi di riattivazione del virus latente o se vi sia qualche serbatoio di replicazione virale a bassi livelli durante tutto il follow-up. L’idea di utilizzare quanto appreso sull’immunità di questi macachi per aumentare ulteriormente queste risposte è interessante e ci stiamo pensando. Comunque, i dati che abbiamo mostrato a Miami suggeriscono che il controllo della carica virale a seguito della terapia migliori con il passare del tempo e quindi, anche in virtù del risultato recentemente pubblicato dal gruppo di Louis Picker, è importante continuare il follow-up onde vedere se, alla lunga, l’infezione possa essere eliminata spontaneamente dalle risposte immunitarie che abbiamo descritto. Ci tengo a precisare però che non vi sono macachi che non hanno risposto al ciclo combinato di ART/auranofin/BSO, entrambi i macachi sottoposti a questo trattamento hanno poi mostrato un controllo a lungo termine della viral load nonché ricostituzione immunitaria. Per quanto il numero di tali macachi sia limitato, la slide che precede le conclusioni mostra un’analisi statistica che indica come ottenere il 100% di successo terapeutico in tutti i macachi trattati con auranofin e BSO (e solo in quelli, in tutta la coorte) sia con tutta probabilità dovuto ad un reale effetto terapeutico e non al caso.
 ).
).